A termodynamiikan toinen pääsääntö määrää, mitkä ehdot ovat olemassa lämpöä muuntaa työksi lämpömoottoreissa ja jääkaapeissa. Se käsittelee myös määritelmää haje ilmiönä, joka pystyy mittaamaan hiukkasten hajoamista fysikaalisissa järjestelmissä.
Lue myös: Kalorimetria - fysiikan haara, joka tutkii lämmönvaihtoa
Tämän artikkelin aiheet
- 1 - Yhteenveto termodynamiikan toisesta pääsäännöstä
- 2 - Mikä on termodynamiikan toinen pääsääntö?
-
3 - Termodynamiikan toisen pääsäännön sovellukset
- Termodynamiikan toinen pääsääntö lämpömoottoreissa
- Jääkaappien termodynamiikan toinen pääsääntö
- 4 - Entropia ja termodynamiikan toinen pääsääntö
-
5 - Termodynamiikan toisen pääsäännön kaavat
- Lämpökoneet ja jääkaapit
- Jääkaapit
- Esimerkkejä kaavojen soveltamisesta
- 6 - Carnot-sykli
- 7 - Termodynamiikan lait
- 8 - Ratkaistiin harjoituksia termodynamiikan toisesta pääsäännöstä
Yhteenveto termodynamiikan toisesta pääsäännöstä
Termodynamiikan toista pääsääntöä edustavat Clausius- ja Kelvin-Planck-lauseet.
Clausiuksen lausunto käsittelee lämmön virtausta kuumemmasta kappaleesta kylmempään kappaleeseen.
Kelvin-Planckin lausunto koskee lämpölaitteiden kyvyttömyyttä muuntaa kaikkea lämpöään tehdä työtä.
Termodynamiikan toista pääsääntöä sovelletaan lämpömoottoreihin ja jääkaappeihin.
Carnot-sykli on lämpömoottorien suurin hyötysuhde.
Carnot-syklissä on neljä vaihetta: palautuva isoterminen laajeneminen, palautuva adiabaattinen laajennus, palautuva isoterminen puristus ja palautuva adiabaattinen puristus.
Carnot'n lause viittaa tuottoon Carnot koneet.
Mikä on termodynamiikan toinen pääsääntö?
Termodynamiikan toinen pääsääntö on a laki, joka käsittelee termodynaamisissa prosesseissa esiintyviä rajoitteita. Sen esittivät fyysikot Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) ja Max Planck (1858-1947), kuten alla nähdään:
Fyysikko ja matemaatikko Rudolf Clausius totesi, että lämmön johtuminen tapahtuu korkeamman lämpötilan kappaleesta alhaisemman lämpötilan kappaleeseen. alhaisempi lämpötila, joten ei ole luonnollista, että käänteinen prosessi tapahtuu, joten on tarpeen suorittaa työtä tämän järjestelmä. Siinä hän totesi:
On mahdotonta toteuttaa prosessia, jonka ainoa vaikutus on lämmön siirtäminen kylmemmästä kappaleesta kuumaan.|1|
Matemaattinen fyysikko William Thomson, joka tunnetaan nimellä Lord Kelvin, yhdessä fyysikko Max Planckin kanssa, totesi 100 %:n hyötysuhteen omaavien lämpölaitteiden mahdottomuuden, koska lämpöhäviö tulee aina olemaan.
Älä nyt lopeta... Julkisuuden jälkeen on muutakin ;)
Termodynamiikan toisen pääsäännön sovellukset
Termodynamiikan toista pääsääntöä sovelletaan lämpömoottoreihin ja jääkaappeihin.
Termodynamiikan toinen pääsääntö koneissa lämpö
Kohteeseen Lämpökoneet pystyvät muuttamaan lämmön työksi. Kuuma lähde toimittaa lämpöä lämpökoneeseen, joka muuttaa sen työksi. Loput lämmöstä, jonka se lähettää kylmälähteeseen alla olevan kuvan mukaisesti:
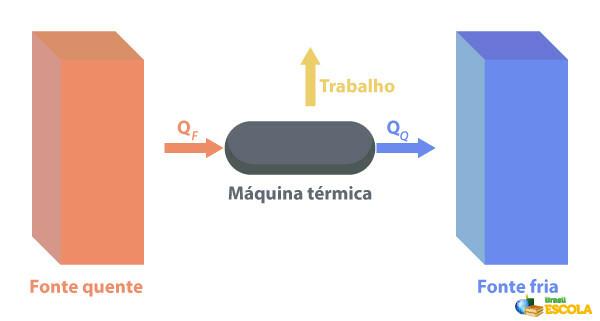
Joitakin esimerkkejä lämpökoneista ovat: höyry- ja kerosiiniturbiinit suihkukoneissa, polttomoottorit, lämpöydinreaktorit.
Jääkaappien termodynamiikan toinen pääsääntö
Jääkaapit ovat koneita Ne toimivat päinvastoin kuin lämmittävät moottorit., jossa ne poistavat lämpöä alueelta, jossa on lämpötila alhaisempi lämpötila ja syötä se alueelle, jossa lämpötila on korkeampi. Koska tämä ei ole luonnollista, koneen on suoritettava sähköenergiaa käyttäviä töitä alla olevan kuvan mukaisesti:
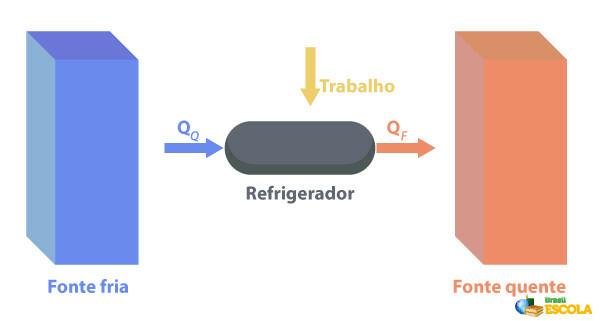
Joitakin esimerkkejä jääkaapeista ovat jääkaapit ja ilmastointilaitteet.
Entropia ja termodynamiikan toinen pääsääntö
A Termodynamiikan toinen pääsääntö ehdottaa entropian olemassaoloa, yksi fyysinen määrä on vastuussa fyysisen järjestelmän hiukkasten hajoamisasteen tai järjestelmän peruuttamattomuuden asteen mittaamisesta. lämpömoottoreissa mukana olevat termodynaamiset prosessit, jotka ovat spontaani, väistämätön, peruuttamaton ja laaja. Tällä on mahdollista vain tarkkailla ja hillitä prosessien volatiliteettiastetta. Kun entropia kasvaa, myös järjestelmän epäjärjestyksen aste kasvaa.
A Entropianimikkeistö on kreikkalaista alkuperää ja tarkoittaa "muutosta"., "muutos", jota käytetään siten Fyysinen ilmaisemaan satunnaisuutta ja epäjärjestystä. Entropia voidaan laskea kaavalla:
\(∆S=\frac{∆U}T\)
\(∆S\) on entropian muutos, mitattuna [J/K].
\(∆U\) on sisäisen energian muutos jouleina [J] mitattuna.
T on lämpötila kelvineinä [K] mitattuna.
Tilastollisesta näkökulmasta entropia lasketaan kaavalla:
\(S=k\cdot ln\ Ω\)
S on entropia, mitattuna [J/K].
k on Boltzmannin vakio, se kannattaa \(1,4\cdot 10^{-23}\ J/K\).
Ω on järjestelmän mahdollisten mikrotilojen lukumäärä.
Lue myös: Lämmön leviämisprosessit
Termodynamiikan toisen pääsäännön kaavat
Lämpökoneet ja jääkaapit
\(Q_Q=W+Q_F\)
\(Q_Q\) on kuuman lähteen lämpö, mitattuna jouleina [J].
W on lämpökoneen työ, mitattuna jouleina [J].
\(Q_F\) on kylmän lähteen lämpö, mitattuna jouleina [J].
Sitä voivat edustaa:
\(W=Q_Q-Q_F\)
W on lämpökoneen työ, mitattuna jouleina [J].
\(Q_Q\) on kuuman lähteen lämpö, mitattuna jouleina [J].
\(Q_F\) on kylmän lähteen lämpö, mitattuna jouleina [J].
Jääkaapit
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) on jääkaapin tehokkuus.
\(Q_F\) on kylmän lähteen lämpö, mitattuna jouleina [J].
\(Q_Q\) on kuuman lähteen lämpö, mitattuna jouleina [J].
Se voidaan esittää seuraavasti:
\(η=\frac{Q_F}W\)
\(η\) on jääkaapin tehokkuus.
\(Q_F\) on kylmän lähteen lämpö, mitattuna jouleina [J].
W on lämpökoneen työ, mitattuna jouleina [J].
Esimerkkejä kaavojen soveltamisesta
Esimerkki 1: Laske työ, jonka lämpökone tekee syklin aikana, joka vastaanottaa 500 J lämpöä kuumasta lähteestä ja siirtää vain 400 J lämpöä kylmään lähteeseen.
Lämpömoottorin työn laskemiseksi käytämme kaavaa:
\(W=Q_Q-Q_F\)
Korvaa lausunnossa ilmoitetut arvot:
\(W=500-400\)
\(W=100\ J\)
Lämpökoneen teho oli 100 joulea.
Esimerkki 2: Mikä on jääkaapin hyötysuhde, joka vastaanottaa 150 J lämpöä kuumasta lähteestä ja siirtää 50 J lämpöä kylmään lähteeseen?
Jääkaapin tehokkuuden laskemiseksi käytämme kaavaa:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
Korvaamalla lausunnossa annetut arvot, saamme:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
Kerrotaan tuotto 100 %:lla:
\(η=0,5\cdot100%\)
\(η=50\%\)
Jääkaapin hyötysuhde on 50 %.
Carnot sykli
Carnot-sykli oli kehittäjä tiedemies Sadi Carnot (1796-1832), jonka tavoitteena on tunnistaa suurin hyötysuhde, joka voidaan saavuttaa lämpömoottorilla, joka toimii kuuman lähteen ja kylmän lähteen välillä.
Tutkimustensa perusteella Carnot havaitsi, että lämpömoottorin maksimaalisen hyötysuhteen saavuttamiseksi se on välttämätön, jotta hänen prosessinsa olisi palautuva, joten hän kehitti enimmäissaantosyklin, jota kutsutaan sykliksi Carnot ja Sen läpi toimivaa lämpömoottoria kutsutaan Carnot-lämpömoottoriksi.. Koska Carnot-sykli on käännettävä, se voidaan kääntää päinvastaiseksi, ja näin jääkaapit kehitettiin.
Carnot-sykli koostuu käytetystä aineesta riippumatta neljästä prosessista, jotka on kuvattu paineen tilavuuskäyrästössä (p×V), kuten alla olevasta kuvasta näkyy:
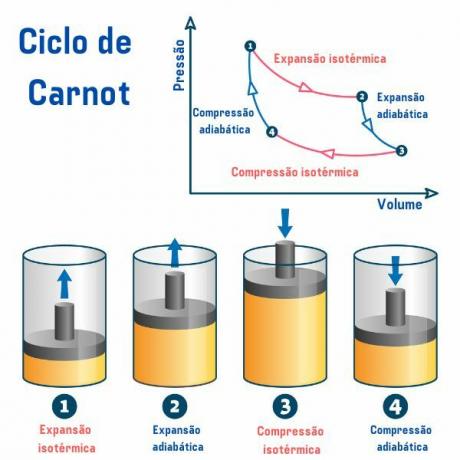
Ensimmäinen prosessi, kohdasta 1 → 2: tapahtuu palautuva isoterminen laajeneminen (prosessi, jossa lämpötila pysyy vakiona), jossa kaasu (tai järjestelmä) toimii ja hankkii osan lämpöä kuumasta lähteestä.
2. prosessi, kohdasta 2 → 3: on adiabaattinen laajeneminen (prosessi, jossa tapahtuu lämmönvaihtoa ulkoisen ympäristön kanssa) palautuva, jossa ei tapahdu lämmönvaihtoa lämmittää lämpölähteillä, mutta kaasu toimii ja sen sisäinen energia vähenee, mikä aiheuttaa kaasun vähenemisen lämpötila.
3. prosessi, kohdasta 3 → 4: tapahtuu palautuva isoterminen puristus, jossa kaasu saa työtä ja luovuttaa osan lämpöä kylmälähteelle.
4. prosessi, kohdasta 4 → 1: tapahtuu palautuva adibaattinen puristus, jossa ei tapahdu lämmönvaihtoa lämpölähteiden kanssa ja kaasu kuumennetaan, kunnes se saavuttaa kuuman lähteen lämpötilan, ja siten asetetaan kosketuksiin sen kanssa, mikä päättyy sykli.
termodynamiikan lait
Termodynamiikan lait ovat neljä lakia, jotka hallitsevat koko tutkimusta termodynamiikka, tutkia tilavuuden, lämpötilan ja paineen sekä muiden fysikaalisten suureiden, kuten lämmön ja energian, välisiä suhteita.
Termodynamiikan nollasääntö: on laki lämpötasapaino, se tutkii lämmönvaihtoa eri lämpötiloissa olevien kappaleiden välillä.
termodynamiikan ensimmäinen pääsääntö: on termodynaamisten järjestelmien energian säilymisen laki, se tutkii lämmön muuttumista työksi ja/tai sisäiseksi energiaksi.
Termodynamiikan toinen pääsääntö: se on laki, joka käsittelee lämpökoneita, jääkaappeja ja entropiaa.
Termodynamiikan kolmas pääsääntö: on laki absoluuttinen nolla, hän tutkii tämän lämpötilan vaikutuksia.
Lue myös: Lämpömoottorien suorituskyky
Ratkaistiin harjoituksia termodynamiikan toisesta pääsäännöstä
Kysymys 1 Määritä Carnot-moottorin kuuman lähteen lämpötila tietäen, että kylmän lähteen lämpötila on 450 K ja sen hyötysuhde on 80 %.
a) 2250K
b) 450K
c) 1500K
d) 900K
e) 3640K
Resoluutio:
Vaihtoehto A. Laskemme kuuman lähteen lämpötilan Carnot-moottorin hyötysuhdekaavan perusteella:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1-\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
kysymys 2 (Cefet-PR) Termodynamiikan toinen periaate voidaan ilmaista seuraavasti: "Konetta on mahdotonta rakentaa jaksoissa toimivaa lämpöenergiaa, jonka ainoa vaikutus on poistaa lämpöä lähteestä ja muuttaa se kiinteästi tehdä työtä". Laajennuksena tämä periaate saa meidät päättelemään, että:
a) Aina on mahdollista rakentaa lämpökoneita, joiden hyötysuhde on 100 %.
b) mikä tahansa lämpökone tarvitsee vain yhden lämmönlähteen.
c) lämpö ja työ eivät ole homogeenisia määriä.
d) mikä tahansa lämpökone ottaa lämpöä kuumasta lähteestä ja hylkää osan tästä lämmöstä kylmään lähteeseen.
e) vain kylmällä lähteellä, joka pidetään aina 0 °C: ssa, voisiko tietty lämpökone muuttaa lämmön kokonaan työksi.
Resoluutio:
Vaihtoehto D. Tämä periaate kertoo meille, että on mahdotonta poistaa kaikkea lämpöä kuumasta lähteestä ja siirtää sitä kylmään lähteeseen.
Huomautus
|1| Fysiikan peruskurssi: Nesteet, värähtelyt ja aallot, lämpö (vol. 2).
Kirjailija: Pamella Raphaella Melo
Fysiikan opettaja
Järjestelmän entropia ei ole muuta kuin sen epäorganisaation asteen mitta. Toinen laki on mahdollista muotoilla entropian käsitteestä.
Tutustu lämpömoottoreiden kiehtovaan historiaan ja niiden pääkäyttöihin.
Tiedätkö mitä lämpökoneet, termodynaamiset syklit ja tehokkuus ovat? Opi lisää näistä tärkeistä termodynamiikan käsitteistä.
Tutustu tekstiin ja opi termodynamiikan ensimmäisen lain määritelmä, katso mitä kaavoja tämä laki käyttää ja tutustu aiheeseen liittyviin ratkaistuihin harjoituksiin.
Isoterminen, isovolumetrinen ja adiabaattinen muunnos. Tapaa heidät!
Tiedätkö mitä termodynamiikka on? Käytä tekstiä saadaksesi selville, mitkä ovat aiheen tärkeimmät käsitteet, ja tutustu termodynamiikan lakeihin.
