Yksi lisäysreaktio on kemiallinen prosessi, jossa epäorgaanisen aineen atomeja lisätään orgaaniseen molekyyliin, jolla on oltava yksi seuraavista ominaisuuksista:
Avoin rakenne, joka sisältää sitoutumista tai pi-linkit;
Kyllästetty suljettu rakenne (vain sigma-linkit);
Suljettu tyydyttymätön rakenne (pi- tai aromaattisella sidoksella).
Orgaaniset yhdisteet, joilla on nämä ominaisuudet, ovat seuraavat Hiilivedyt:
alkeenit;
Alkynes;
Alkadieenit;
Syklanit;
Pyörät;
Aromaatit.
Aikana lisäysreaktio, yksi tai useampi pi-sidos tai sigmasidos (yksinomaan syklanin tapauksessa) rikkoutuu aiheuttaa kahden tai useamman vapaan valenssin (sitoutumiskohtien) ilmestymisen mukana oleviin hiileen, kuten esimerkissä karjua:
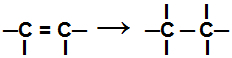
Pi-sidoksen rikkominen alkeenissa
Kun tämä sidos on katkennut, atomien on lisättävä orgaaniseen yhdisteeseen luotuihin uusiin sitoutumiskohtiin. Alla luetellaan niiden tyypit lisäysreaktiot joka voidaan suorittaa orgaanisilla yhdisteillä.
hydraus
Tässä lisäysreaktioorgaanisen yhdisteen lisäksi toinen reagenssi on vetykaasu (H
2). Jokaisessa hiilessä, jossa fissio tapahtuu (sigma- tai pi-sidoksen rikkoutuminen, kuten edellä nähtiin), esiintyy vetyatomin sidos rikkoutuneiden sidosten määrään.Kun suoritamme esimerkiksi syklobutaanin hydrauksen, sigma-sidos rikkoutuu hiilien 1 ja 2 välillä. Sitten vetyatomi sitoutuu jokaiseen näistä hiilistä:
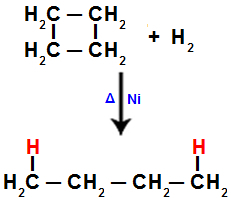
Yhtälö, joka edustaa hydrausta syklobutaanissa
Halogenointi
Orgaanisen yhdisteen lisäksi toinen tämän reagenssi lisäysreaktio on molekyylihalogeeni (kloori-Cl-kaasu2, fluori-F-kaasu2, kiinteä jodi-I2 ja nestemäinen bromi-Br2). Jokaisessa hiilessä, jossa fissio tapahtuu (sigma- tai pi-sidoksen rikkoutuminen, kuten yllä nähdään), on halogeeni viittaamalla katkenneiden yhteyksien määrään.
Siten, kun suoritamme syklopropeenin halogenoinnin (kloorikaasua käyttäen), pi-sidos rikkoutuu hiilien 1 ja 2 välillä. Sitten klooriatomi sitoutuu jokaiseen näistä hiilistä:

Yhtälö, joka edustaa halogenoitumista syklopropeenissa
Lisäysreaktio halogenidin kanssa
Halogenidi on epäorgaaninen vesihappo, jonka muodostavat vetyatomi ja vetyatomi. halogeeni, kuten kloorivetyhappo (HCl), fluorivetyhappo (HF), bromivetyhappo (HBr), happo hydroiodinen (HI).
Klo lisäysreaktio halogenidin kanssa orgaanisen yhdisteen lisäksi toinen reagenssi on halogenidi, siten yksi hiilistä, jossa leikkauksen (sigma- tai pi-sidoksen rikkoutuminen, kuten yllä nähdään) on vastaanotettava vetyatomi, ja toisen tulee vastaan halogenidi.
Mukaan Markovnikovin sääntö, hydratun hiiliatomin (tai pienempään radikaaliin sitoutuneen hiilen) on vastaanotettava vety, ja vähemmän hydratun hiilen (tai suurempaan radikaaliin sitoutuneen hiilen) täytyy saada halogenidi.
Esimerkiksi, kun suoritamme tämän reaktion propeenilla suolahapolla (HCl), pi-sidos rikkoutuu hiilen 1 ja 2 välillä. Sitten vety sitoutuu hiileen 1 (enemmän hydrattu) ja kloori hiileen 2 (vähemmän hydrattu):
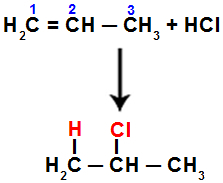
Yhtälö, joka edustaa lisäystä halogenidin kanssa propeenissa
Nesteytysreaktio
Kun vesimolekyyli ionisoituu, se tuottaa hydrroniumkationin (H+) ja hydroksidianioni (OH-). Tästä syystä tässä lisäysreaktioorgaanisen yhdisteen lisäksi toinen reagenssi on vesi. Siten toinen hiilistä, joissa tapahtuu fissio (sigma- tai pi-sidoksen rikkoutuminen, kuten yllä nähdään), saa hydroniumkationin ja toinen hydroksidi-anionin.
Markovnikovin säännön mukaan eniten hydrattu hiiliatomi (tai pienempään radikaaliin kiinnittynyt hiili) on vastaanotettava hydronium, ja vähemmän hydratun hiilen (tai suurempaan radikaaliin sitoutuneen hiilen) on saatava hydroksidi.
Kun hydratoimme esimerkiksi penta-1,4-dieeniä, pi-sidos rikkoutuu hiilen 1 ja 2 välillä ja hiilen 4 ja 5 välillä. Sitten hiilet 1 ja 5 saavat hydroniumin ja hiilet 2 ja 4 saavat hydroksidin:
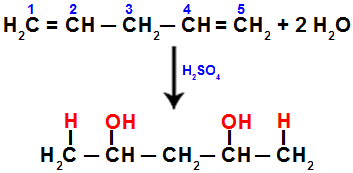
Yhtälö, joka edustaa lisäystä hydrataation kanssa penta-1,4-dieenissä
Minun luona. Diogo Lopes Dias
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-reacao-adicao.htm


