Kp on lyhenne, jota käytetään määrittämään tasapainon vakio osapaineiden suhteen. Tämä vakio toimii esimerkiksi atm-yksikön tasapainon kaasumaisten osallistujien arvojen kanssa.

Yhtälö, joka edustaa kemiallista reaktiota kaasumaisten komponenttien kanssa
Tässä yhtälössä kaikki osallistujat ovat kaasumaisia, joten kun osallistuvalla kaasulla on a osapaine seoksessa, sitä edustaa lyhenne pX.
Kemiallisen tasapainon yhtälöä laadittaessa (pitoisuuden suhteen) tuotteet on sijoitettava osoittajaan ja reagoivat aineet nimittäjään:
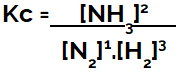
Ammoniakin muodostumisen tasapainon Kc-ilmentyminen
ilmaisu tasapainovakio paineena (Kp) seuraa mallia Kceli reagenssien osapaineet sijoitetaan nimittäjään ja tuotteiden osapaineet osoittajaan:
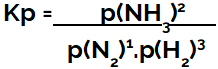
Ammoniakin muodostumistasapainon Kp: n ilmentyminen
Havainto: Jos reaktioyhtälö kemiallinen tasapaino älä esitä kaasumaista osallistujaa, se ei esiinny automaattisesti Kp.
Esimerkki: (PUC-MG) Reaktiolle: 2 CO(g) + O2(g)? 2 CO2(g), CO: n osapaineet(g) se on2(g) tasapainossa ne ovat vastaavasti 0,2 atm ja 0,4 atm. Järjestelmän kokonaispaine on 1,4 atm. Arvo Kp sillä reaktio on:
a) 56.2
b) 40,0
c) 35.6
d) 28.4
e) 25.6
Harjoituksen antamat tiedot ovat:
Hiilimonoksidin osapaine (pCO) = 0,2 atm;
Hiilimonoksidin osapaine (pO2) = 0,4 atm;
Kokonaispaine = 1,4 atm;
Tämän järjestelmän Kp: n määrittämiseksi meidän on suoritettava seuraavat vaiheet:
1. vaihe: Määritä hiilimonoksidin osapaine (pCO2).
Muista vain, että kokonaispaine (pt) on kaikkien osapaineiden summa:
pt = pCO + pCO2 + pO2
1,4 = 0,2 + p (CO2) + 0,4
1,4 - 0,2 - 0,4 = pCO2
pCO2 = 0,8 atm
2. vaihe: Määritä harjoituksen Kp.
Käytä tätä varten vain arvoja tasapainovakion Kp lausekkeessa:
Kp = (pCO2)2
(pCO)2.(pöly2)1
Kp = (0,8)2
(0,2)2.(0,4)1
Kp = 0,64
0,04.0,4
Kp = 0,64
0,016
Kp = 40 atm-1
Kirjailija: Me. Diogo Lopes Dias
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kp.htm

