Jotkut metallit eivät ole luonteeltaan vapaita, ja ne on hankittava laboratoriomenettelyillä. Yksi tehokkaista ja taloudellisista menetelmistä metallien puhdistamiseksi on elektrolyysi. Elektrolyysi tapahtuu elektrolyyttikennoissa, kaksi elektrodia kytkettynä tasavirta-generaattorin liittimiin.
Tiedetään, että elektrolyyttikennossa on katodi ja anodi, katso kunkin määritelmä:
Katodi: Negatiivinen elektrodi houkuttelee kationeja, ja tässä tapahtuu kationin pelkistys.
anodi: Positiivinen elektrodi, joka houkuttelee anioneja, ja siksi tässä anioni hapettuu.
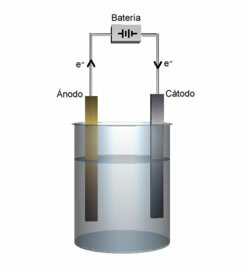
Anodi ja katodi esittely.
Kuparin puhdistus
Luonnossa esiintyvässä kuparissa on epäpuhtauksia, kuten hopea, rauta, kulta, sinkki. Elektrolyysin avulla on mahdollista eristää tämä metalli, jolloin se saadaan puhtaassa muodossa, seuraa prosessia:
- Epäpuhdas kupari toimii anodina ja kuparisulfaatin vesiliuos toimii elektrolyytinä, joka on elektrolyysikennon sisällä. Solun katodi on itse kupari puhtaana.
- Kupari siirtyy anodista katodiin epäpuhtauksien pysyessä liuoksessa. Kupari puhtaassa tilassa kertyy katodiin ja voidaan siten käyttää.
Kirjoittanut Líria Alves
Valmistunut kemian alalta
Brasilian koulutiimi
Katso lisää!
Elektrolyysireaktiot
Elektrolyysituotteet
Elektrolyysi - Fysikaalis-kemiallinen - Kemia - Brasilian koulu
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/purificacao-metais-atraves-eletrolise.htm
