Sulamispiste ja kiehumispiste edustavat lämpötilaa, jossa aine muuttaa tilaa tietyssä paineessa.
Sulamispisteen tapauksessa aine muuttuu kiinteästä tilasta nestemäiseksi. Kiehumispiste viittaa muutokseen nestemäisestä tilasta kaasumaiseen tilaan.
Esimerkiksi jää alkaa muuttua vedeksi nestemäisessä muodossa, kun sen lämpötila on 0 ° C. Siksi veden sulamispiste on 0 ° C (1 atmosfäärin paineessa).
Veden on vaihdettava nesteestä höyryksi lämpötilaan 100 ° C. Siten veden kiehumispiste on 100 ° C (1 atmosfäärin paineessa).

Fuusiopiste
Kun kiinteässä tilassa oleva aine vastaanottaa lämpöä, sen molekyylien sekoitusaste kasvaa. Tämän seurauksena myös sen lämpötila nousee.
Saavutettuaan tietyn lämpötilan (sulamispiste) molekyylien sekoitus on sellainen, että ne rikkovat sisäiset siteet atomien ja molekyylien välillä.
Tässä vaiheessa aine alkaa muuttaa tilaansa ja siirtyy nestemäiseen tilaan, jos se saa edelleen lämpöä.
Aikana Fuusio sen lämpötila pysyy vakiona, koska vastaanotettua lämpöä käytetään yksinomaan tilan vaihtamiseen.

Vaiheen vaihtamiseksi tarvittavaa lämpöä massayksikköä kohti kutsutaan piilevä lämpö fuusion (Lf) ja on aineen ominaisuus.
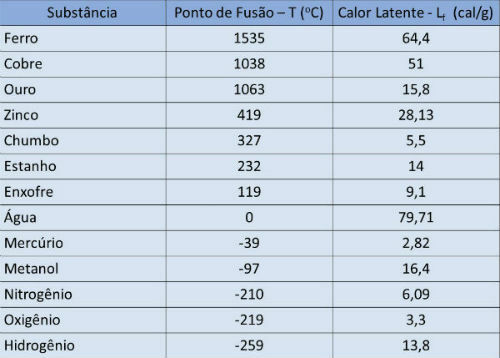
Sulamispiste ja piilevä lämpöpöytä
Alla olevassa taulukossa ilmoitetaan sulamispisteen lämpötila ja joidenkin aineiden piilevä lämpö ilmakehän paine.
Kiehumispiste
THE kiehuva sille on ominaista nopea siirtyminen nesteestä kaasumaiseen tilaan, jolloin nesteen sisään muodostuu höyryjä (kuplia).
Kuten fuusiossa, on lämpötila (kiehumispiste), jossa tietty aine muuttuu nestemäisestä kaasumaiseksi.
Tämän tapahtuessa aineen täytyy saada lämpöä. Lämpötila pysyy vakiona koko vaihemuutoksen ajan.
piilevä lämpö höyrystyminen (Lv) on lämmön määrä massayksikköä kohti, joka tarvitaan aineen vaiheen muuttamiseen.
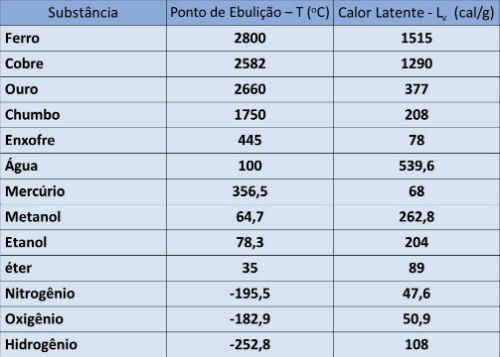
Kiehumispiste ja piilevä lämpöpöytä
Alla olevassa taulukossa ilmoitetaan joidenkin aineiden kiehumispisteen lämpötila ja piilevä höyrystymislämpö ilmakehän paineessa.
Painehäiriöt
Sulamispisteen ja kiehumispisteen lämpötila riippuu aineelle kohdistetusta paineesta.
Yleensä aineiden määrä kasvaa, kun ne fuusioituvat. Tämä tarkoittaa sitä, että mitä korkeampi paine, sitä korkeampi lämpötila aineelle vaihtaa faasi.
Poikkeus tapahtuu joillakin aineilla, mukaan lukien vesi, joka vähentää sen tilavuutta sulatettaessa. Tässä tapauksessa korkeampi paine alentaa sulamispistettä.

Paineen lasku aiheuttaa tietyn aineen kiehumispisteen olevan matalampi, mikä tarkoittaa, että aine kiehuu alemmassa lämpötilassa.
Esimerkiksi paikoissa merenpinnan yläpuolella vesi kiehuu alle 100 ° C: n lämpötilassa. Tämän seurauksena ruoanlaitto kestää paljon kauemmin näissä paikoissa kuin paikoissa merenpinnan tasolla.
Lue myös:
- Fyysisen tilan muutokset
- Lämpömittarit
- Lämpömittarit - Harjoitukset
- Veden fyysiset tilat
- Vaihekaavio
- Kiinteytyminen
- Tiivistyminen
- Kollektiiviset ominaisuudet
- Jaksolliset ominaisuudet
- Haihdutus
- Jaksollisen harjoitukset



