pH edustaa vetyionipotentiaalia ja pOH on liuosten hydroksiionipotentiaali.
Nämä ovat logaritmisia asteikkoja, joita käytetään näytteen happamien ja emäksisten ominaisuuksien mittaamiseen.
Ne muodostavat arvot vaihtelevat välillä 0 - 14, ja ne saatiin veden ionitasapainosta.
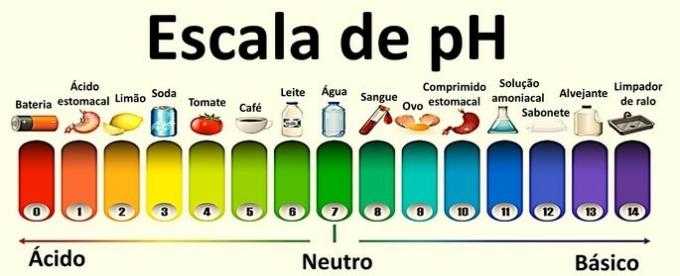
Neutraalin liuoksen pH on 7. Alle 7: n arvot luokittelevat liuokset happamiksi, kun taas 7: n jälkeen liuokset ovat emäksisiä.
PH-arvon avulla on mahdollista löytää vastaava pOH-asteikolta vain tekemällä vähennys.
Ioninen vesitasapaino
Vesimolekyylillä on kyky ionisoida yhtälön mukaan:
Täällä meillä on ionitasapaino, koska prosessi on palautuva ja ionit voivat myös tulla yhteen ja muodostaa uudelleen vesimolekyylin.
Toinen tapa osoittaa syntyvä tasapaino on autoionisaatio.
Vesimolekyyli tuotti hydroniumioneja (H3O+) ja hydroksyyli (OH-) hajottamalla toinen molekyyli.
Veden ionituote (Kw)
Veden ionitasapainon vakio on:
Koska vesi on puhdasta nestettä, sen pitoisuus otetaan yhdeksi eikä se häiritse vakioarvoa. Siksi lausekkeesta tulee:
O - ioninen tuote Vesi é .
Tämä lauseke saa symbolin Kw (W tulee englanninkielisestä sanasta vesi - vettä) ja kuten tasapainovakio, se vaihtelee lämpötilan mukaan.

PH: n ja pOH: n määrittäminen
25 ° C: n lämpötilassa veden ionituote on:
Puhtaan veden ionisaatiossa 1 mol H: ta3O+ muodostuu 1 moolilla OH: ta- .
Pian,
Koska nämä arvot ovat erittäin pieniä, päätettiin käyttää kologaritmien arvoja, jotka vastaavat vaihdettua merkkiä sisältävää logaritmia.
Kologaritmin soveltaminen veden ionituotteeseen on:
Voidaan havaita, että jos tiedämme liuoksen pH: n, pOH-arvo voidaan löytää vähentämällä ensimmäinen arvo arvosta 14.
Happamuus ja ratkaisujen emäksisyys
Neutraali liuos: hydrroniumionien pitoisuus on yhtä suuri kuin hydroksyylien.
| [H3O+] = 1,0. 10-7 mol / l | pH = 7 |
| [vai niin-] = 1,0. 10-7 mol / l | pOH = 7 |
Esimerkki: puhdas vesi.
happoliuos: hydrroniumionien pitoisuus on suurempi kuin hydroksyylien.
| [H3O+] |
pH |
| [vai niin-] |
pOH |
Esimerkki: sooda, sitruuna ja tomaatti.
perusratkaisu: hydroksyylipitoisuus on suurempi kuin hydroniumionien.
| [H3O+] |
pH |
| [vai niin-] |
pOH |
Esimerkki: muna, saippua ja valkaisuainetta.
pH-laskenta
Tanskalainen kemisti Peter Lauritz Sorensen (1868-1939) loi käsitteen vetypotentiaalista ilmaisemaan liuoksen happamuus H+.
Katso alla olevasta taulukosta a happo:
| Alkuperäinen molaarisuus | 0,020 | 0 | 0 |
| ionisaatio | 0,001 | 0,001 | 0,001 |
| Molaarisuus tasapainossa | 0,019 | 0,001 | 0,001 |
Esimerkissä meillä on H-ionien pitoisuus+ é 0,001. Siksi liuoksen pH on:
[H+] = 0,001 = 10-3
pH = - log 10-3 = 3
Koska liuoksen pH on alle 7, tämä liuos on hapan.
Yhteenveto pH: sta ja pOH: sta
| Määritelmät | pH: liuoksen vetyionipotentiaali. | |
|---|---|---|
| pOH: liuoksen hydroksyylionionipotentiaali. | ||
| yleinen kaava | pH + pOH = 14 | |
| Ratkaisut | Neutraali | pH = pOH = 7 |
| hapan |
pH pOH> 7 |
|
| perusasiat |
pOH pH> 7 |
|
| pH-laskenta | pH = - log [H+] | |
| POH: n laskeminen | pOH = -log [OH-] |
Harjoitukset pH: lla ja pOH: lla
1. Mahahapon mehun, suolahapon (HC2) vesiliuoksen, pH on noin 2. Siksi jokaisessa mahalaukun mehulitrassa olevan HC2: n massa grammoina on
Tiedot: Moolimassa (g / mol) H = 1, C3 = 35,5
a) 7,3 · 10-2
b) 3,65 · 10-1
c) 10-2
d) 2
e) 10
Oikea vaihtoehto: b) 3,65 · 10-1.
1. vaihe: laske H-ionien pitoisuus+.
2. vaihe: lasketaan HCl: n moolimassa.
3. vaihe: Laske suolahapon massa litraa mahalaukun mehua.
2. (UEMG) Monien puhdistusaineiden rakenne on ammoniakki. Yhden näistä tuotteista on merkitty pH-arvoon 11. Tämä tarkoittaa, että hydroksoniumkationien ja hydroksyylianionien pitoisuudet tässä tuotteessa ovat vastaavasti:
1: een. 10-3 ja 1. 10-11
b) 1. 10-11 ja 1. 10-7
c) 1. 10-11 ja 1. 10-3
d) 1. 10-11 ja 1. 10-11
Oikea vaihtoehto: c) 1. 10-11 ja 1. 10-3.
a) VÄÄRIN. Nämä pitoisuudet vastaavat liuosta, jonka pH = 3.
b) VÄÄRIN. Vaikka H-pitoisuus+ osoittavat, että liuoksen pH on 11, OH-ionien pitoisuus- on väärin, kuten sen pitäisi olla 3, koska: pOH = 14 - pH.
c) OIKEA. pH = 11 ja pOH = 3, koska pH + pOH = 14.
d) VÄÄRIN. Vaikka H-pitoisuus+ osoittavat, että liuoksen pH on 11, OH-ionien pitoisuus- on väärin, kuten sen pitäisi olla 3, koska: pOH = 14 - pH.
a) 0,1 mol / l NaOH
b) NaCl 0,5 mol / l
c) H2VAIN4 1,0 mol / l
d) 1,0 mol / l HCI
e) 0,2 mol / l KOH
Oikea vaihtoehto: e) KOH 0,2 mol / L.
a) VÄÄRIN. Liuos on emäksinen, koska sen pH on suurempi kuin 7, mutta sen vaihtoehtojen pH ei ole korkeampi.
b) VÄÄRIN. NaCl on suola, koska se on vahvan happo- ja emäksisen reaktion tuote. Siksi sen pH on neutraali.
c) VÄÄRIN. Rikkihappo on vahva happo, joten sen pH on matala.
d) VÄÄRIN. Kloorivetyhappo on vahva happo, joten sen pH on matala.
e) OIKEA. Liuos on emäksinen, koska sen pH on yli 7.