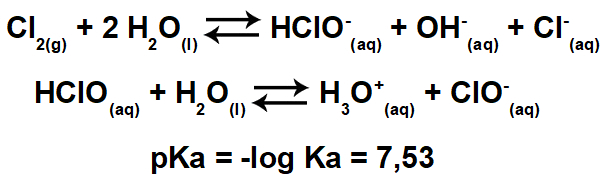Saldolämpö on tila, jossa keho löytää itsensä samalämpötila kuin heidän ympäristöönsä. Havaitaan, että kaikki ruumiinsa, jotka ovat korkeammissa lämpötiloissa kuin naapurit, pyrkivät antamaan heille lämpöä itsestään, kunnes molemmat alkavat tuottaa saman lämpötilan.
Katsomyös:Termologian perusteet
Terminen tasapaino ja termodynamiikan nollalaki
Terminen tasapaino on termodynamiikan nollalain takana oleva keskeinen käsite. Tällaisessa laissa säädetään, että siinä tapauksessa, että kaksi termodynaamista järjestelmää, THE ja B, ovat termisessä tasapainossa kolmannen termodynaamisen järjestelmän kanssa, Çsitten, THE ja B ne ovat myös termisessä tasapainossa.
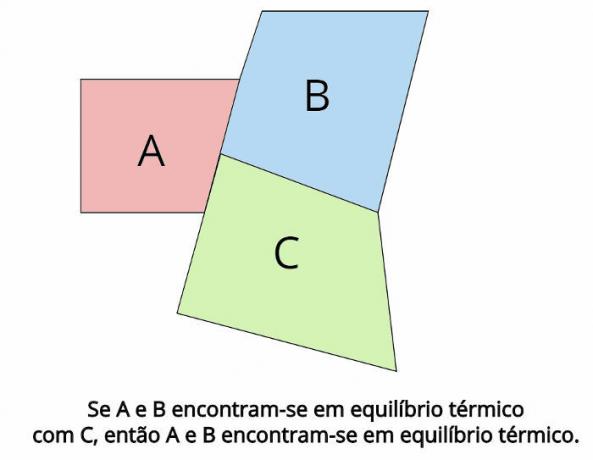
Lämpötasapainossa kunkin ruumiin lopullisten lämpötilojen on oltava samat: TTHE = TB = TÇ
Katso, mitä termodynamiikan nollalain lausunto vahvistaa:
“Jos kaksi elintä on termisessä tasapainossa kolmannen ruumiin kanssa, niin ne ovat termisessä tasapainossa keskenään. "
Toinen tapa ymmärtää terminen tasapaino perustuu elinten sisäiseen energiaan. Sisäinen energia tai yksinkertaisesti lämpöenergia on fyysinen määrä
suoraansuhteellinen à lämpötila kehosta. Siksi, jos saman termodynaamisen järjestelmän sisällä on kappaleita, joiden lämpötila on erilainen, niillä on erilaiset moduulit sisäistä energiaa ja siirtää siksi osan energiasta niiden välillä, kunnes heidän energioidensa välillä ei ole eroa. sisäinen. Haluatko tietää enemmän siitä, mikä on sisäinen energia ja mitkä ovat sen ominaisuudet? Käytä artikkelia: Sisäinen energia.Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
lämmön ja lämmön tasapaino
Lämmönsiirto tapahtuu aina spontaanisti korkeimman lämpötilan kehosta alimman lämpötilan kehoon. Tämä energian siirto lämmön muodossa voi tapahtua esimerkiksi prosessien kautta ajo-, konvektio ja säteily.
Ajo: Lämmönsiirto kappaleiden välillä tapahtuu erityisesti kiinteissä aineissa. Tämän tyyppisessä johtamisessa ei tapahdu massansiirtoja. Tämän tyyppinen lämmönsiirto selittää, miten lämpö tasapaino tapahtuu esimerkiksi metalleissa.
Konvektio: Se on lämmönsiirto, joka tapahtuu nesteissä. Tässä lämmönsiirtotilassa tapahtuu massansiirto, kun lämmitetty neste liikkuu muodostaen konvektiovirtoja, kunnes kaikki neste saavuttaa lämpötasapainon.
Säteily: Se on lämmön siirtyminen sähkömagneettisten aaltojen kautta, joten tämä prosessi tapahtuu, vaikka kehon ja toisen ruumiin välillä ei ole fyysistä väliainetta eri lämpötiloissa. Siirtyvä lämpö tässä tapauksessa vastaa sähkömagneettisia aaltoja, joissa on vähemmän energiaa kuin - näkyvä valo, siten lämpösäteily, sijaitsee infrapuna.
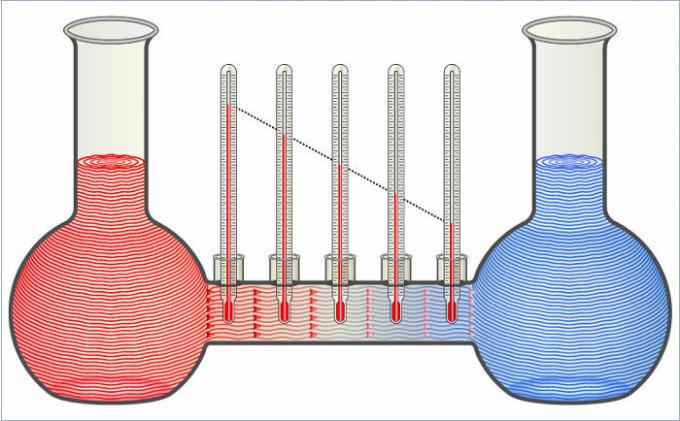
Kuvan kaksi nestettä siirtävät lämpöä toisilleen, kunnes niiden lämpötilat ovat samat.
Haluatko tietää enemmän siitä, miten kukin lämmönsiirtoprosessi tapahtuu? Käytä artikkelia: Lämmön etenemisprosessit.
järkevä lämpö
kun on erosisäänlämpötila kahden ruumiin tai kehon ja sen ympäristön välillä tapahtuu lämmönvaihto niiden välillä spontaanisti, niin että korkeamman lämpötilan runko jäähtyy ja alemman lämpötilan rungot lämpenevät, kunnes ne kaikki saavuttavat lämpötilan sisään saldolämpö.
Lämmön määrää, joka vaihdetaan kappaleiden välillä eri lämpötiloissa, kutsutaan järkevä lämpö ja tämä määrä voidaan laskea alla olevan kuvan mukaisesta kaavasta:
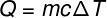
Q - lämpö (kalkki tai J)
m - massa (g tai kg)
ç - ominaislämpö (cal / gºC tai J / kg. K)
ΔT - lämpötilan vaihtelu (° C tai K)
Edellä esitetyssä kaavassa on tärkeää korostaa nimen suuruutta ominaislämpö. tällainen suuruus mittaa energiamäärä massaa kohti, jonka aineen on tuotettava tai absorboitava, jotta sen lämpötila vaihtelee 1 ° C. Esimerkiksi puhtaan veden tapauksessa ja normaaleissa paineolosuhteissa lämpötilan vaihtelemiseksi 1 ° C: lla tarvitaan 1,0 kaloria kutakin grammaa kohti vettä.
Siten kaikki aineet, joilla on ollut lämpökontakti toistensa kanssa, pyrkivät saavuttamaan saldolämpö ajan mittaan spontaanisti jotkut tarvitsevat kuitenkin suuremman määrän energiaa tekemään niin, ja tämä vaikuttaa suoraan lämpötilaan saavuttaakseen lämpötasapainon.
lukeamyös:Mikä on lämpötila?
piilevä lämpö
On mahdollista, että lämmönvaihdon yhteydessä ympäröivän ruumiin paine, lämpötila ja tilavuus aiheuttavat sen fyysisen tilan muutoksen. Nämä muutokset tapahtuvat lämpötilavakio (elimille, jotka koostuvat yhdestä aineesta, ilman epäpuhtauksia), toisin sanoen näiden elinten lämpötila ei muutu huolimatta siitä, että ne vastaanottavat tai antavat lämpöä ulkoiselle ympäristölle.
Tämä on mahdollista vain, koska kaikkea tässä vaihdettua energiaa käytetään molekyyliesi konformaation muuttamiseen. Siitä hetkestä lähtien, kun energiaesteet on "ylitetty" ja kaikki kehon sisällöt ovat toisessa fyysisessä tilassa, Keho jatkaa lämmönvaihtoa ympäristönsä kanssa, ellei tietysti sen lämpötila ole yhtä suuri kuin ulkona oleva lämpötila.
O piilevä lämpö voidaan laskea alla olevan kuvan mukaisesta kaavasta, tarkista se:
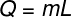
Q - piilevä lämpö (kalkki tai J)
m - massa (g tai kg)
L - spesifinen piilevä lämpö (cal / g tai J / kg)
Lämpötasapainokaava
Jos haluamme selvittää mikä on lämpötilasisäänsaldo joissakin termodynaamisissa järjestelmissä on välttämätöntä, että pidämme kyseistä järjestelmää a järjestelmääneristetty, toisin sanoen meidän on oletettava, että mitään lämpöä ei vaihdeta tämän järjestelmän naapureiden kanssa.
Tästä ehdosta voimme sanoa, että koko vaihdettu lämmön määrä vaihtuu vain tämän järjestelmän muodostavien kappaleiden välillä, lämpöhäviöt huomioimatta esimerkiksi astian seinämille. Tässä tapauksessa sanomme, että kontilla on lämpökapasiteetti merkityksetön, eli se ei ime lämpöä.
Kuvittele seuraava tilanne: kaada jääkuutioita kupilliseen kuumaa teetä, jonka lämpökapasiteetti on vähäinen. Lämpötasapainolämpötilan määrittämiseksi meidän on tehtävä järjestelmän alkuolosuhteiden tuntemisen lisäksi joitain huomioita:
Kaikki kuuman teen jäälle antama lämpömäärä imeytyy siihen täysin, koska kupin lämpökapasiteetti on vähäinen.
Meidän on jätettävä huomiotta ilman ja muun ympäristön lämpöhäviöt, jotta tämä kuppi teetä voidaan ymmärtää suljetuksi termodynaamiseksi järjestelmäksi.
Tällä tavalla voimme todeta, että kuuma tee luovutti koko jään vastaanottaman lämmön määrän, ja kirjoitimme tämän kaavan lämpötaseiden laskemiseksi:
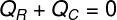
QR - Lämpö vastaanotettu
QÇ - lämpö annettu
(QÇ), viittaa lämmön määrään, jonka kuuma tee siirtää siihen asetettuihin jääkuutioihin. Jo saatu lämpö (QR) on näiden jääkuutioiden saaman lämmön määrä. Tällä lämpömäärällä on kaksi luonnetta: lämpö herkkä ja kuuma piilevä, koska päästäkseen lämpötasapainoon jääkuutiot todennäköisesti sulavat.
Lämpötasapainolämpötilan määrittäminen
Määritetään lämpötasapainolämpötila seuraavasta tilanteesta:
Kuppi, jolla on vähäinen lämpökapasiteetti ja joka sisältää 200 ml (200 g) teetä alkulämpötilassa 70 ° C, saa 10 g jäätä -10 ° C: n lämpötilassa. Määritä järjestelmän terminen tasapainolämpötila (oletetaan, että teen ominaislämpö on yhtä suuri kuin veden ominaislämpö):
Tiedot:
çVESI = 1,0 cal / g ° C
çICE = 0,5 cal / g ° C
LICE = 80 cal / g
Ensinnäkin katsomme, että tee antoi kaiken jään vastaanottaman lämmön:

Seuraavaksi on tarpeen tarkentaa, mitkä lämpömuodot annettiin ja vastaanotettiin:
Tee: Tee antoi vain kohtuullista lämpöä (Qs), koska hänen fyysinen kunto ei ole muuttunut.
Jäätä: Jää oli alun perin -10 ° C: ssa, joten se sai kohtuullista lämpöä (Qs) kunnes lämpötila on 0 ºC, sitten se saa piilevää lämpöä (QL) nestemäiseksi. Nesteen tullessa se sai piilevää lämpöä (Qs), kunnes se saavuttaa termisen tasapainon (TF) teen kanssa.
Kääntämällä yllä analysoitu yhtälön muodossa meillä on seuraava laskettava ratkaisu:
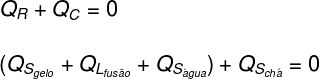
Korvaamalla harjoituksen antamat tiedot yllä olevassa yhtälössä meidän on ratkaistava seuraava laskelma:
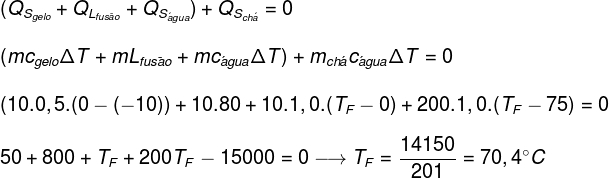
Edellä tehdyn laskelman mukaan tee + jääjärjestelmän tasapainolämpötilan tulisi olla noin 70,4 ° C.
Lämpötasapainotesti
Kahden kappaleen välisen termisen tasapainon testaamiseksi voimme suorittaa useita kokeita. Yksinkertaisin näistä liittyy kuitenkin a: n käyttöön kalorimetri se on a lämpömittari. Kalorimetri on adiabaattinen säiliö (joka ei salli lämmön kulkua), jonka lämpökapasiteetti on noinmerkityksetön, kuten esimerkiksi styroksilla vuorattu ruukku, joka on hyvä lämpöeristin.

Kalorimetriä käytetään järjestelmän sisäisen lämpötilan vaihtelun mittaamiseen.
Terminen tasapaino ja elämä maapallolla
O saldolämpö sillä on keskeinen rooli maanpäällisessä elämässä. Ilman kasvihuonekaasuja maapallon ilmakehässä suurin osa lämpösäteily planeetan jättää sen levittäen avaruuteen. Ajan myötä tämä aiheuttaisi valtavan jäähdytyksen koko planeetalle, mikä aiheuttaisi valtamerien jäätymisen ajan myötä.
Lisäksi valtamerillä on keskeinen rooli saldolämpö planeetan. Sen suurenmoisuuden ansiosta pasta ja lämpöäerityinen, valtamerillä on valtava kapasiteettilämpö, toisin sanoen heidän on vastaanotettava valtavia määriä lämpöä lämpötilan muuttamiseksi. Tästä syystä he pystyvät säätelemään maapallon lämpötilaa erittäin tehokkaasti. Alueet, jotka ovat kaukana valtameristä ja joilla on vähän vettä, ovat yleensä suuria lämpöalueet, kuten aavikoissa, jotka ovat erittäin kuumia päivällä ja jäätyvät yöllä.
Siksi saldolämpö se on perustavanlaatuinen prosessi fyysisten, kemiallisten ja biologisten prosessien ylläpitämiseksi planeetalla ja siten välttämätön elämän olemassaololle maapallolla.
Minun luona. Rafael Helerbrock