Klo kovalenttiset sidokset, kutsutaan myös molekyyli- tai homopolaariset sidoksetovat niitä, joita esiintyy elektronegatiiviset elementiteli on taipumus vastaanottaa elektroneja, jolloin muodostuu jakamalla elektroneja valenssikuoristaan.
Kovalenttista sidosta voi esiintyä seuraavien elementtien välillä: vety, ei-metallit ja puolimetallit. Metallit eivät koskaan osallistu tämän tyyppiseen sidontaan.
Tarkastellaan yksinkertaista esimerkkiä kovalenttisesta sidoksesta: vetykaasun muodostavaa sidosta (H2):
H + H → H2
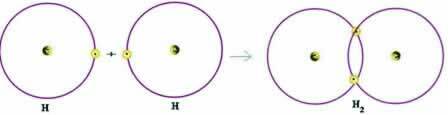
Huomaa, että molempien atomien oli vastaanotettava elektroni valenssikuorensa täydentämiseksi - Octet-säännön mukaisesti - ja tällä tavoin pysyäkseen vakaina. Siksi he jakoivat elektroninsa, ja tällä tavoin molemmilla oli kaksi elektronia, heillä oli täydellinen K-kuori ja hankittu jalokaasuheliumin kokoonpano.
Tämä elektronien jakaminen erottaa tämän tyyppisen sidoksen ionisidoksesta, jossa elektroninsiirto tapahtuu.
Katso alla olevasta kuvasta kaksi muuta esimerkkiä tästä tapauksesta:
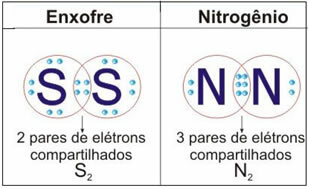
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Tämän tyyppisessä sidoksessa muodostuu molekyylejä, jotka voidaan edustaa niiden vastaavilla molekyylikaavat, eli yksinkertaisin esitys, joka osoittaa, kuinka monta atomia kustakin elementistä on molekyylissä. Joitakin esimerkkejä molekyylikaavoista ovat: H2, S2, O2, ei2, H2O, CO2, jne.
Kovalenttinen sidos voidaan esittää kahdella muulla kaavalla:
- Sähköinen kaava tai Lewis-kaava: tässä kaavassa esiintyvät myös kunkin atomin valenssikuoren elektronit ja elektronisten parien muodostuminen. Näitä elektroneja symboloivat merkit . tai x;
- Tasainen rakennekaava tai Couper-rakennekaava: näyttää elementtien linkit, jolloin kukin jaettu pari vastaa viivaa. Jos se on vain viiva, kutsumme sitä yhdeksi linkiksi; jos niitä on kaksi, kaksoissidos; ja jos on kolme viivaa, kolmoissidos.
Katso muita esimerkkejä kovalenttisista sidoksista, joita nämä kolme kemiallista kaavaa edustavat:
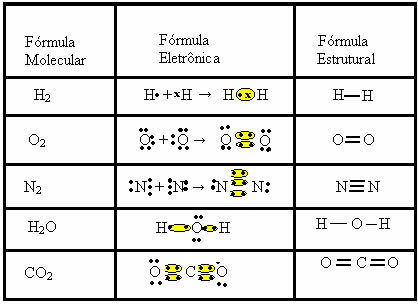
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Kovalenttiset sidokset"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. Pääsy 27. kesäkuuta 2021.



