Ranskalainen kemisti Joseph Louis Proust (1754-1826) jatkoi huolellisia kokeita, jotka koskivat tiettyjen reaktioiden komponenttien massaa.
Esimerkiksi vettä muodostavat alkuaineet ovat vety ja happi. Proust havaitsi, että tässä veden muodostumisreaktiossa vety reagoi aina hapen kanssa vakiona ja määritellyssä suhteessa, joka oli vastaavasti 1: 8. Katso, miten tämä tapahtuu alla:

Huomaa, että riippumatta siitä kuinka paljon käytettyjä elementtejä on, osuus on aina sama.
Proust totesi, että näin ei ollut vain vedessä, vaan kaikissa muissa aineissa.
15,06 g kuparisulfidia (CuS) muodostetaan esimerkiksi saattamalla 10,00 g metallikuparia (Cu) reagoimaan 5,06 g rikkiä (S). Joten jos kaksinkertaistamme kuparimäärän (joka nousee 20,0 grammaan) ja jos haluamme kaiken kuparin reagoivan, Rikin määrä on myös kaksinkertaistettava 10,12 grammaan, jolloin kokonaismäärä on 30,12 g sulfidi.
Jos nyt lisätään määrä, joka ei ole suhteessa, ylimääräinen määrä jää jäljelle, se ei reagoi. Huomaa tämä alla:
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
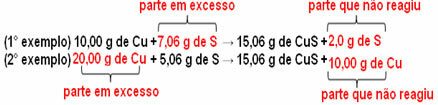
Huomaa, että reaktio tapahtuu vain määritetyn osuuden mukaisesti. Siksi Proust totesi vuonna 1799, että kun useat aineet yhdistyvät muodostaen yhdisteen, tämä tapahtuu aina määritellyssä massasuhteessa.
Joten hän loi lain, jota kutsutaan Proustin laki, Laki vakio-osuuksista tai Määriteltyjen osuuksien laki, joka todetaan seuraavasti:

Tämä laki ja Lavoisierin laki (Joukkosuojelulaki) on nimetty Painolakit, koska ne puhuvat joukkoina mukana olevia aineita.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Proustin laki tai pysyvien osuuksien laki"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/lei-proust-ou-lei-das-proporcoes-constantes.htm. Pääsy 27. kesäkuuta 2021.