Hapettumis-pelkistysreaktiolle on tunnusomaista samanaikainen menetys ja elektronien menetys, koska muut vastaanottavat heti atomin, ionin tai molekyylin menettämät elektronit.
Jos haluat ymmärtää, katso esimerkki:
Kuparisulfaattiliuos (CuSO4 (aq)) on sininen Cu-ionin läsnäolon vuoksi2+ liukenee siihen. Jos laitamme metallisen sinkkilevyn (Zns) tässä ratkaisussa voi ajan mittaan havaita kaksi muutosta: liuoksen väri muuttuu värittömäksi ja sinkkilevylle ilmestyy metallinen kuparikerros.
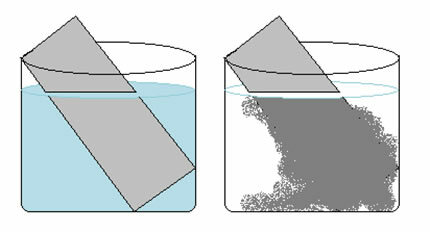
Siksi tässä tapauksessa tapahtuva reaktio on seuraava:
Zns + CuSO4 (aq) → Cus + ZnSO4 (aq)
tai
Zns + Cu2+(tässä) + Käyttöjärjestelmä42-(tässä) → Cus + Zn2+(tässä) + Käyttöjärjestelmä42-(tässä)
tai vielä
Zns + Cu2+(tässä) → Cus + Zn2+(tässä)
Huomaa, että elektronien siirtyminen sinkistä kupariin tapahtui. Analysoimalla erikseen kussakin näistä elementeistä tapahtunut muutos, meillä on:
- Zns → Zn2+(tässä)
Sinkki menetti 2 elektronia siirtymällä metallisesta sinkistä kationiin. Siinä tapauksessa, sinkki on hapettunut.
- Perse2+(tässä) → Cus
Kuparin kanssa tapahtui päinvastainen, se sai 2 elektronia, siirtyen kupari II -kationista metallikupariin. Kupari on vähentynyt.
Tämä selittää kaksi havaittua muutosta, kun liuos muuttui värittömäksi, koska kupari-ionit muuttuivat metallikupariksi, joka kerrostui sinkkilevylle.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Koska elektronien menetys ja vahvistus tapahtui samanaikaisesti, tämä reaktio on esimerkki redox-reaktiosta, ja sen avulla voimme luoda seuraavat käsitteet, jotka toistuvat kaikille muille tämän reaktioille tyyppi:

Reagoivin metalli hapettuuSiten ehdotetussa esimerkissä sinkki on reaktiivisempi kuin kupari.
Toinen redoksireaktio, johon voidaan vedota, tapahtuu, kun laitamme magnesiumia tai alumiinia suolahappoliuokseen. Näissä reaktioissa kloorivetyhapon vety saa 3 elektronia alumiinista (tai 2 elektronia magnesiumista) ja siirtää sen H-kationista+ vetykaasulle (H2), kun taas metallista tulee kationi:
2 Als + 6 H+(tässä) → 2 Al3+(tässä) + 3H2 g)
mgs + 2 H+(tässä) → Mg2+(tässä) + H2 g)
Metallit hapettavat ja vety pelkistyvät. Alla on luku, joka osoittaa, että magnesiumin lisääminen kloorivetyhappoon aiheuttaa a kuohuviiniä, joka johtuu vetykaasun vapautumisesta, ja magnesium katoaa sellaisenaan kulutettu.
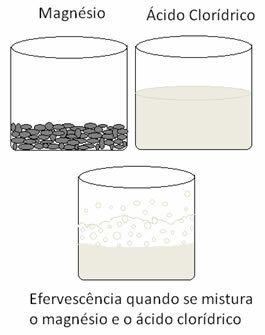
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Hapetusreaktiot"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao.htm. Pääsy 28. kesäkuuta 2021.
Kemia
Turvatyynyn käyttö, kuljettajien suojaamiseksi suunniteltu laite, sähköinen impulssi, kemiallinen hajoamisreaktio, törmäys, natriumatsidin kemiallinen seos, auton puskurissa olevat anturit, alkalisilikaatti, kaasu typpeä.
Kemia

Valoherkät linssit, hapetus-pelkistysreaktiot, elektronien menetys tai voitto, fotosynteettiset linssit aurinkolasissa, valokromaattisen lasin koostumus, tetraedriset happiatomit, hopeakloridin kiteinen rakenne, ultraviolettivalo, hopeametalli

