THE sp-tyyppinen hiilihybridisaatio se tapahtuu vain, kun se muodostaa kaksi pi-sidosta (π) ja kaksi sigmasidosta (σ). Tässä tapauksessa on siis kaksi mahdollisuutta: hiili voi muodostaa kaksi kaksoissidosta tai yhden ja kolmen sidoksen, kuten alla on esitetty:
Teksti "sp-tyypin hybridisaatio3”Näyttää yksityiskohtaisesti, miten hiilihybridisaatio tapahtuu. Muistaminen: hybridisaatio on puhtaiden atomi- orbitaalien "sekoittaminen", jotka ovat peräisin toisistaan vastaavia, mutta alkuperäisistä puhtaista orbitaaleista poikkeavia hybridi-atomi-orbitaaleja. Joten tämä tapahtuu hiilen orbitaaleissa, jotka olivat alun perin edustettuina näin:
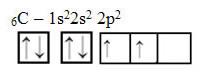
Energian vastaanottamisen myötä elektroni (jota kuvaa nuoli) 2s-kiertoradalta ylennetään 2p-kiertoradalle:
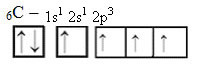
Tällä tavalla hiilellä on neljä parittamatonta orbitaalia, joka pystyy muodostamaan neljä kovalenttista sidosta, ei vain kahta.
Sp-tyyppisen hybridisaation tapauksessa tiedämme, että kaksi sidosta tulee pi; nämä esiintyvät puhtaissa p-orbitaaleissa, kun taas kaksi muuta orbitaalia, jotka ovat sp-hybridit, muodostavat jäljellä olevat sigmasidokset.
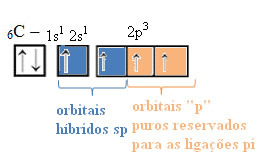
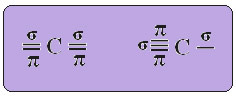
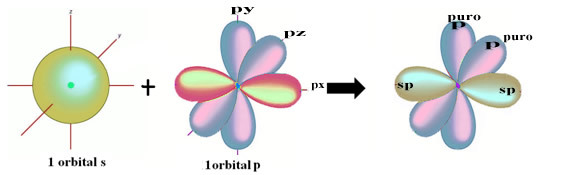
Tämän s: n ja p-orbitaalin välisen hybridisaation spatiaalinen esitys, joka aiheuttaa hybridin sp-orbitaalin, voidaan esittää seuraavasti:
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Yllä olevassa kuvassa on hyvin selvää, että on olemassa kaksi puhdasta orbitaalia, jotka tekevät pi-sidokset.
Otetaan esimerkkinä syanidikaasumolekyyli (HCN), jota käytetään Yhdysvalloissa kaasukammioissa vankeille, joille on annettu kuolemanrangaistus. Sen rakennekaavan antaa:
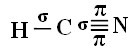
Mitä tulee hiileen, sen atomi-orbitaalit on jo osoitettu, katso nyt vety- ja typpi-orbitaaleja:
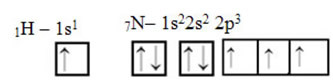
Huomaa, että parittamaton vety-kiertorata, joka suorittaa sigmasidoksen, on ”s”, jota alueellisesti edustaa ympyrä; ja typpi-orbitaalit ovat “p” -tyyppiä, joita edustaa kolme kaksoismunaa (kukin tilakentässä: x, y, z). Siten HCN-molekyylin rakenne on esitetty seuraavasti:
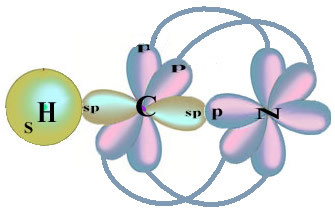
Tässä formaldehydirakenteessa olevien sidosten tyypistä meillä on:
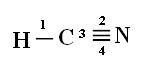
Liitännät: 1 = σs-sp
2 = σp-sp
3 = 4 = πp-p
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Sp-tyyppinen hybridisaatio"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp.htm. Pääsy 28. kesäkuuta 2021.