optinen isomeeri on eräänlainen spatiaalinen isomerismi, jonka päätavoitteena on tutkia epäsymmetriaa edustavien molekyylien käyttäytymistä eli toistensa kanssa päällekkäisyyksiä.

vasen käsi peilikuva
Molekyylejä, jotka eivät ole päällekkäisiä (epäsymmetrisiä molekyylejä), voidaan verrata oikeaan käteen ja sen peilikuvaan. Yllä olevassa kuvassa vasemman käden peilikuva on oikea käsi, joka ei ole päällekkäinen.
Tärkeimmät erot esiintyvien molekyylien välillä optinen isomeria ovat vaikutuksessa, jonka ne aiheuttavat tai eivät polarisoitu valo, kykenevät taipumaan valoon tai olematta sitä suhteessa niiden fysikaalisiin ja kemiallisiin ominaisuuksiin.
Väittää, että aineella on optinen isomeria, meidän on etsittävä sen molekyyleistä vähintään yhden läsnäoloa epäsymmetrinen hiili (kutsutaan myös kiraaliseksi hiileksi), joka on hiili, jolla on neljä erilaista ligandia, kuten seuraavassa esimerkissä:

Hiili, jossa on neljä erilaista sideainetta
Yllä olevassa hiilessä on vety (H), metyyli (CH) ligandeja3), bromia (Br) ja etyyliä (H3C-CH2) ja on siten kiraalinen hiili.
Katso nyt tutkitut isomeerityypit Optinen isomeria:
Aktiiviset optiset isomeerit
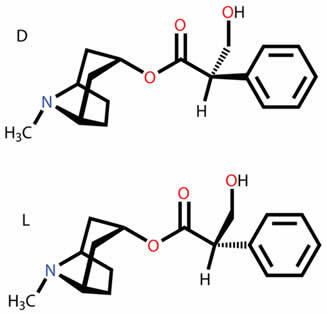
Kutsutaan myös optiset antipodit, enantiomorfit tai kiraaliset molekyylitovat orgaanisia molekyylejä, joilla on kyky siirtää polarisoidun valon suunta vasemmalle tai oikealle.
Orgaanisen yhdisteen molekyyliä, joka pystyy taipumaan valoa oikealle, kutsutaan a oikeakätinen. Saman orgaanisen yhdisteen molekyyliä, joka pystyy siirtämään valoa vasemmalle, kutsutaan levorotary.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Jokaisella orgaanisella yhdisteellä, jolla on kiraalista hiiltä, on automaattisesti oikeakätinen molekyyli ja vasenkätinen molekyyli. Kuitenkin, jos tietyssä orgaanisessa yhdisteessä on enemmän kuin yksi kiraalinen hiili, meidän on käytettävä tiedemies Van't Hoffin ehdottama kaava oikeakätisten molekyylien määrän määrittämiseksi ja levoreiras. Katso:
IOA = 2Ç
IOA = optisesti aktiiviset isomeerit;
C = kiraalisten hiilien lukumäärä molekyylissä.
Passiiviset optiset isomeerit
Kutsutaan myös raseeminen seos, inaktiivisissa optisissa isomeereissä meillä on sama määrä oikean- ja vasemmanpuoleisia molekyylejä säiliössä. Tällä seoksella ei ole kykyä siirtää polarisoidun valon suuntaa joko vasemmalle tai oikealle.
Tutkija Van't Hoffin ehdottaman säännön mukaan orgaanisen yhdisteen muodostamien raseemisten seosten lukumäärän määrittämiseen käytetään vain seuraavaa ilmaisua:
IOI = 2Ç
2
IOI = optisesti inaktiiviset isomeerit;
C = kiraalisten hiilien lukumäärä molekyylissä.
meso-isomeeri
meso-isomeeri on molekyyli, jolla on kaksi yhtä suurta kiraalista hiiltä, eli molemmilla hiileillä on samat neljä ligandia, kuten seuraavassa esimerkissä:

Viinihapolla on meso-isomeeri
Hiilen 2 ja 3 ligandit ovat täsmälleen samat: hydroksyyli (OH), karboksyyli (COOH), vety (H) ja hiilihydroksi-karboksyyliryhmä (CHOHCOOH).
Koska meso-isomeerillä on kaksi yhtä suurta kiraalista hiiltä, toisen hiilen vaikutus polarisoituun valoon kumotaan toisen hiilen vaikutuksesta. Siksi se on optisesti inaktiivinen isomeeri.
Minun luona. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Mikä on optinen isomerismi?"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria-optica.htm. Pääsy 28. kesäkuuta 2021.
Kemia
Tiedä mistä erityyppiset taso- ja avaruusisomeerit ovat kyse, kuten toiminta, sijainti, ketju, tautomerismi, metamerismi, cis-trans-geometrinen ja optinen isomeeri.