Vuonna 1911 Uuden-Seelannin tiedemies Ernest Rutherford esitteli tiedeyhteisölle hänen atomimalli. Rutherfordin malli, jota kutsutaan myös aurinkokuntamalliksi, oli kolmas atomihistorian historiassa (kaksi ensimmäistä olivat Dalton ja Thomsonin malli) ja sitä pidettiin mallina, joka stimuloi koko aineen aineosaa, atomia koskevan tiedon kehittymistä.
Rakentaminen Rutherford-malli aloitti Röntgen ja radioaktiiviset päästöt, jotka huipentuvat säteilyn käyttöön inertissä esineessä, toisin sanoen sellaisessa, joka ei reagoi helposti.
Rutherfordin suorittama koe
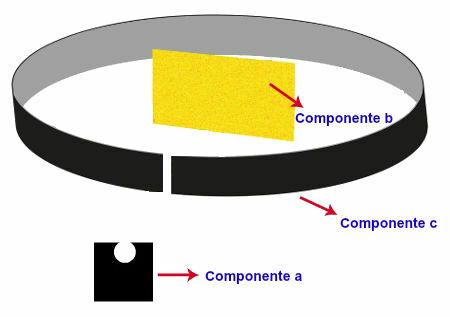
Rutherfordin suorittamassa kokeessa oli seuraava laite ja organisaatio:
Komponentti a - näyte poloniumista (emitteri alfa-säteily) sijoitettu lyijylohkoon. Tässä lohkossa oli pieni reikä, jonka läpi säteily kulki;
Komponentti b: erittäin ohut kultainen terä sijoitettu lyijykotelon eteen;
Komponentti c: Metallinen levy, joka on peitetty fluoresoivalla materiaalilla (sinkkisulfidi), sijoitettu kultalevyn taakse, viereen ja vähän eteenpäin.
Esitys Rutherfordin tekemästä kokeesta
Rutherfordin kokeen tulokset
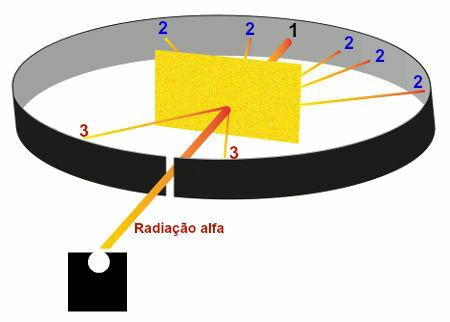
Esitys Rutherford-kokeessa havaituista tuloksista
Alue 1: alue, joka sai suuren osan poloniumin lähettämästä alfa-säteilystä, mikä osoitti, että nämä säteilyt ylittivät kultalevyn kärsimättä merkittäviä poikkeamia;
Alue 2: useita kultalevyn takana sijaitsevia alueita, jotka saivat pienen määrän alfa-säteilyä, mutta eivät olleet säteilyn poistoaukko lyijykotelossa, mikä osoitti, että nämä säteilyt kärsivät suuresta poikkeamasta ylityksen jälkeen kulta;
Alue 3: kultalevyn edessä olevat alueet, jotka saivat erittäin pienen määrän alfa-säteilyä, mikä osoitti, että osa alfa-säteilystä törmäsi levyn kanssa ja palautui takaisin.
Rutherfordin kokeen tulosten tulkinnat
Tulkinta alueesta 1: Koska suuri osa alfa-säteilystä kulki kultalevyn läpi ilman esteitä, tämä tarkoittaa, että atomit oli suuria tyhjiä tiloja (sähköpallo), eli alueita, joilla ei ollut mitään kykyä vaikuttaa säteilyyn alfa;
Tulkinta alueesta 2: Pieni poikkeavuus alfasäteilyä kulki lähellä atomin positiivista aluetta (ydintä), todennäköisesti pienikokoista, mikä edisti poikkeamaa.
Tulkinta alueesta 3: Koska erittäin pieni määrä alfasäteilyä palautui, se tarkoittaa, että ne törmäsivät erittäin pieneen atomin alueeseen, jolla oli positiivinen ominaisuus.
Rutherfordin atomimallin ominaisuudet
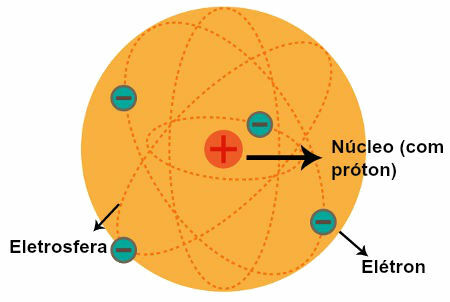
Esitys Rutherfordin atomimallista
Rutherfordin tekemien havaintojen jälkeen hän muotoili atomimallinsa, jolla oli seuraavat ominaisuudet:
a) Ydin (jota on verrattu aurinkokunnan aurinkoon)
Atomin keskeinen alue, jolla on:
positiiviset hiukkaset ( protonit);
pieni äänenvoimakkuus;
suurempi massa;
suurempi tiheys atomin.
b) Sähköpallot (joita on verrattu aurinkokunnan planeettojen kuvaamiin kiertoradoihin)
Atomin alueet, joilla on:
valtavat tyhjät tilat niiden välillä;
negatiiviset hiukkaset ( elektronit).
Minun luona. Diogo Lopes Dias
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/o-atomo-rutherford.htm