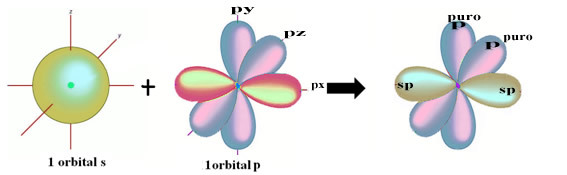
Kovalenttisia sidoksia voi esiintyä molekyyli- tai datatiivi- ja koordinaattimuodossa.
Molekyylikovalenttinen sidos
Tässä sidoksessa atomit liitetään niiden elektronien jakamisen vuoksi, sitten ympyrän osoittamat elektroniset parit ilmestyvät:
Kahden kloori (Cl) atomin molekulaarinen kovalenttinen sidos.
Jokainen samanaikaisesti muodostettu elektroninen pari kuuluu kahteen atomiin. Molekyylit ovat sähköisesti neutraaleja rakenteita, koska elektronien vahvistusta tai häviämistä ei ole, ne ovat vain yhteisiä.
Vesi on molekyyliyhdiste, joka koostuu kahdesta vetyatomista (H2) ja yksi happi (O).
datiivi ja koordinoi kovalenttinen sidos
Tämä sidos noudattaa oktettiteoriaa: Atomit yhdistyvät yrittäen hankkia kahdeksan elektronia valenssikuoresta eli jalokaasujen elektronisesta konfiguraatiosta.
Siten atomi, joka on jo saavuttanut elektronisen vakauden, liittyy toiseen, joka tarvitsee elektroneja valenssikuoren loppuunsaattamiseksi. Esimerkki tästä sidoksesta on, kun rikkiatomi sitoutuu kahteen happiatomiin muodostaen rikkidioksidia (SO
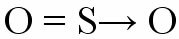
Rikkiatomi (S) saa oktettinsa muodostamalla kaksoissidoksen vasemmalla sijaitsevan hapen kanssa (koordinoitu sitoutuminen), mutta samalla oikealle sijoitettu happi tarvitsee elektroneja sen loppuunsaattamiseksi oktetti. Sitten ilmestyy datatiivinen kovalenttinen sidos, jota edustaa pieni vektori (nuoli). Nuoli osoittaa, että “s” lahjoittaa elektroniparin “O”.
Tarkastellaan elektronien jakamista rikkitrioksidiyhdisteen (SO3).
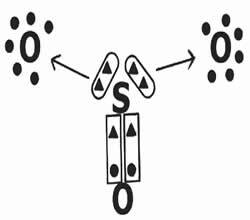
Huomaa, että keskuselementti (rikki) muodostaa kaksoissidoksen (koordinoitu) yhden hapen kanssa saavuttaen elektronisen vakauden (kahdeksan elektronia valenssikuoressa). Toisaalta se lahjoittaa kaksi elektroniparia oksygeeneille (nuolen osoittama datatiivinen sidos →) yrittäen täydentää oktettia.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Kirjoittanut Líria Alves
Valmistunut kemian alalta
Katso lisää!
Metalliliitäntä
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
SOUZA, Líria Alves de. "Kovalenttisidos "; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/ligacao-covalente.htm. Pääsy 27. kesäkuuta 2021.