Atomit ovat äärettömän pieniä hiukkasia, jotka muodostavat kaiken maailmankaikkeuden aineen. Ajan myötä ajatus atomirakenteen muutoksesta muuttui tutkijoiden tekemien uusien löytöjen mukaan. Saat lisätietoja tästä tekstistäAtomimallin kehitys.
Malli on todellisuuden esitys (ei itse todellisuus), joten atomimallit ovat esityksiä atomin pääkomponentit ja sen rakenne ja selittävät aineen tietyn fysikaalisen ja kemiallisen käyttäytymisen. Tämä tehdään, koska ihmisen ei ole vielä mahdollista nähdä eristettyä atomia edes ultramikroskoopeilla.
Saadaksesi käsityksen siitä, kuinka pieni atomi on, tiedä se Pienin tavallisessa mikroskoopissa näkyvä hiukkanen sisältää yli kymmenen miljardia atomia! Atomi on niin pieni, että, jos laitamme miljoonan heistä vierekkäin, emme saavuta hiusten paksuus.
Miellekartta: Atom
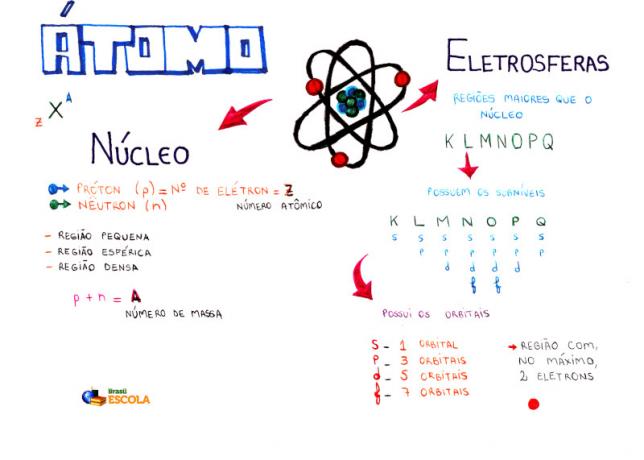
* Voit ladata mielikartan PDF-muodossa. Klikkaa tästä!
Atomimalleista Rutherford-Bohrin malli on parhaiten lukiossa nykyisin käytetty atomin rakenteen ja ominaisuuksien ymmärtämiseen. Tämän mallin mukaan atomin rakenne koostuu kahdesta pääosasta: ydin ja sähköpallo.

Kaksi pääosaa atomin rakenteesta - sähköpallo ja ydin
* Ydin: Muodostuu atomin keskiosaksi, se on kompakti, massiivinen ja erittäin tiheä, sen lisäksi, että sen muodostavat suuremman massan hiukkaset, jotka ovat protoneja ja neutroneja.

Kuva protoneista ja neutroneista, jotka muodostavat atomin ytimen
- protonit: ne ovat hiukkasia, joilla on positiivinen sähkövaraus (suhteellinen varaus = +1; varaus kulona (C) = +1,602. 10-19) ja sen suhteellinen massa on yhtä suuri.
Se, että protonit muodostavat ytimen ja antavat sille yleisen positiivisen varauksen, havaittiin Eugen Goldstein, vuonna 1886 muuttamalla Crookesin ampullia ja joitain kokeita. Hän näki, että erittäin korkeiden jännitteiden vallitessa ilmestyi päästöjä (anodisäteet - jäännökset kaasun atomista, jotka olivat polttimon sisällä ja joiden elektronit repivät irti sähköpurkauksesta). Sijoittamalla sähkö- tai magneettikenttä polttimon ulkopuolelle nämä säteet taipuivat kohti negatiivista napaa. Tämä tarkoitti, että oli positiivisia subatomisia hiukkasia, joita kutsuttiin protoneiksi.
Myöhemmin, Ernest Rutherford (1871-1937) suoritti tekstissä kuvatun kokeen Rutherfordin Atom, joka sai hänet löytämään protonin sijainti: ytimessä.
- Neutronit: ne ovat hiukkasia, joiden massa on yhtä suuri kuin protonit (1), mutta kuten nimestä käy ilmi, ne ovat neutraaleja, ts. niillä ei ole sähkövarausta.
Neutronit löysi vuonna 1932 James Chadwick (1891-1974), joka huomasi, että radioaktiivisen berylliumin ydin lähetti neutraaleja hiukkasia, joiden massa oli suunnilleen sama kuin protonien massa (itse asiassa se on hieman suurempi).
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Ytimen halkaisija riippuu atomin protonien ja neutronien määrästä, mutta keskimäärin se on noin 10-14 kuukausi ja 10-15 m.
Atomin ydin keskittyy käytännössä koko atomin massaan, mikä on hyvin pieni osa: sekä protoni että neutroni ovat noin 100 000 kertaa pienempiä kuin itse atomi! Kuvittele vertailun vuoksi, että suurennamme vedyn alkuaineen (jolla on vain.) Atomin ydintä (protoni) tennispallon kokoon, lähin elektroni olisi noin kolmen kilometrin päässä etäisyys! Vaikka atomi laajennettaisiin 14-kerroksisen rakennuksen korkeuteen, sen ydin olisi seitsemännen kerroksen pelkän suolan kokoinen. Se on todella jotain hämmästyttävää, etkö usko ?!
* Sähköpallo: On alue, jolla elektronit pyörivät ytimen ympäri. Huolimatta siitä, että se on paljon suurempaa tilavuutta kuin ydin, se on käytännössä tyhjä, koska kukin elektroni on 1836 kertaa pienempi kuin 1 protoni. Siksi atomin massa on käytännössä kaikki ytimessä. Elektronit ovat hiukkasia, joilla on negatiivinen sähkövaraus (-1).
Elektronit löysi vuonna 1897 Joseph John Thomson (1856-1940), elokuvan luoja Thomsonin atomimalli. Thomsonin kokeilu näkyy yksityiskohtaisesti tekstissä Thomsonin kokeilu sähköpurkauksilla, mutta lyhyesti sanottuna hän käytti edellä mainittua Crookes-ampullia ja huomasi, että katodisäteet olivat aina positiivinen napa, mikä osoitti, että atomilla oli negatiivisia hiukkasia, joita kutsuttiin elektronit.
Elektronit pyörivät ytimen ympärillä miljardeja kertoja sekunnin miljoonasosassa muodostaen atomin ja saaden sen käyttäytymään ikään kuin se olisi kiinteä.
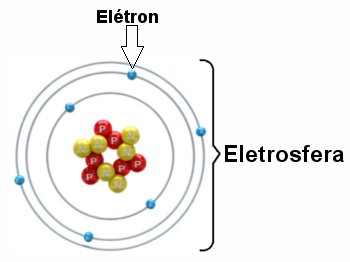
Kuva sähköpallosta, jossa on kolme elektronista kerrosta ja elektronit pyörivät ytimen ympäri.
Lyhyesti sanottuna voimme tehdä taulukon erottaa kolme pääatomia, jotka ovat osa atomin rakennetta:

Kolmen tärkeän subatomisen hiukkasen - protonien, neutronien ja elektronien - massa ja sähkövaraus
Kaikkien kemiallisten alkuaineiden atomit koostuvat näistä kolmesta subatomisesta hiukkasesta. Erilainen kemiallinen alkuaine on määrä, jossa nämä hiukkaset esiintyvät, erityisesti protonien määrä ytimessä, jota kutsutaan atomiluvuksi. Jatka sen tutkimista tekstin kautta. Kemiallinen alkuaine.
* Minun mielikartta, Diogo Lopes
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Kemia
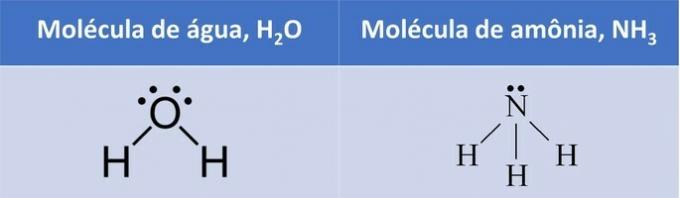
Aineen, veden, syaanivetykaasun, hiilidioksidin, ammoniakin, vedyn, heliumin, aineiden luokitus yksinkertaiset yhdisteaineet, seokset, seoksen faasit, homogeeninen seos, seos heterogeeninen.