Yleensä puhtaita aineita ovat tuskin löydetty luonteeltaan eristettyinä, jotka löytyvät muodossa seokseteli liittyy muihin aineisiin. Tämä tarkoittaa, että me ja melkein kaikki ympärillämme ovat esimerkkejä kaikkein vaihtelevimpien puhtaiden aineiden seoksista.
Tässä tekstissä opitaan, mikä se on ja mitkä ovat puhtaiden aineiden ja seosten luokitukset.
puhtaita aineita
puhtaita aineita ovat materiaaleja, joilla on kemiallinen koostumus ja ominaisuudet vakiot fysikaaliset ja kemialliset, koska ne eivät muutu vakiopaineessa ja lämpötilassa.
Puhtaat aineet voidaan yleensä luokitella kahdella tavalla:
a) Yksinkertaiset aineet
Ne ovat kemiallisia yhdisteitä, jotka muodostavat saman kemiallisen elementin atomit. Esimerkiksi:
→ H2 (Vetykaasu)
Vetykaasumolekyylit muodostuvat kemiallisen vetyelementin kahdesta atomista, joten se on yksinkertainen aine.
→ O3 (Otsonikaasu)
Otsonikaasumolekyylit muodostuvat hapen kemiallisen alkuaineen kolmesta atomista, joten se on yksinkertainen aine.
On myös mahdollista, että saman kemiallisen elementin atomit muodostavat täysin erilaiset yksinkertaiset aineet, allotropit. Esimerkki
allotropia näin on kemiallisella alkuaineella Happi, joka muodostaa kaasuaineista happea (O2) ja otsonikaasu (O3).Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
B) yhdisteaineet
Ne ovat kemiallisia yhdisteitä, jotka muodostavat eri kemiallisten alkuaineiden atomit. Esimerkkejä:
→ CO2 (Hiilikaasu tai hiilidioksidi)
Hiilidioksidimolekyylit muodostuvat yhdestä alkuaineen hiilestä ja kahdesta hapen atomista. Koska kemialliset alkuaineet ovat erilaisia, se on yhdisteaine.
→ kmnO4 (Kaliumpermanganaattia)
O ionikaava kaliumpermanganaatin muodostuu yhdestä kaliumelementin atomista, yhden alkuaineen mangaaniatomista ja neljästä alkuaineen hapen atomista.
Miellekartta: Puhdas aine ja seos

* Voit ladata mielikartan PDF-muodossa. Klikkaa tästä!
Seokset
Sekoita se on kahden tai useamman eri aineen yhdistyminen (riippumatta siitä, ovatko ne yksinkertaisia vai yhdistettyjä). Sen fysikaaliset ominaisuudet (sulamispiste, kiehumispiste, tiheys, sitkeys jne.) Ovat erilaisia ja vaihtelevia (ei kiinteitä) verrattuna sen sisältäviin aineisiin.
Esimerkiksi veden ja natriumkloridin seoksella on täysin erilainen sulamispiste verrattuna veden sulamispisteisiin (0OC) ja natriumkloridi (803OC) yksin.
a) Homogeeniset seokset
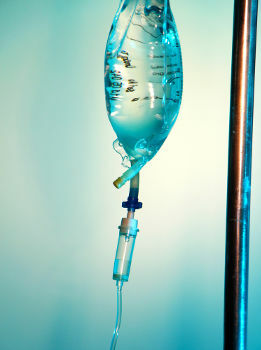
Suolaliuos on homogeeninen seos, joka muodostuu vedestä, glukoosista ja natriumkloridista
Homogeenisilla seoksilla on vain yksi vaihe (yksi visuaalinen ulkonäkö). Ne muodostuvat, kun yhdellä materiaalilla on kyky liuottaa toinen. Esimerkkejä:
vesi ja natriumkloridi;
vesi ja glukoosi;
bensiini ja etanoli;
ilmakehän ilma (happikaasu, typpikaasu, hiilidioksidi, vesihöyry jne.);
etikkahappo ja vesi;
maaöljy (bensiini, kerosiini, voiteluöljy jne.);
suolaliuos.
b) Heterogeeniset seokset

Maito on heterogeeninen seos, koska siinä on nestefaasi (vesi) ja kiinteä faasi (rasva)
Heterogeenisillä seoksilla on enemmän kuin yksi faasi (kaksi tai useampia visuaalisia näkökohtia). Ne muodostuvat, kun yksi materiaali ei liueta toista. Esimerkkejä:
Graniitti;
Maito;
Veri;
Vesi ja hiekka;
Vesi tämä on Leo;
Vesi ja bensiini.
* Victor Ricardo Ferreiran miellekartta
Kemian opettaja
Minun luona. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Puhtaat aineet ja seokset"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/mistura-e-substancias-puras.htm. Pääsy 28. kesäkuuta 2021.
Kemia

Katso kemian peruskäsitteiden, kuten aine, energia, aine, seos, runko, esine, massa, tilavuus ja järjestelmä, määritelmä.

