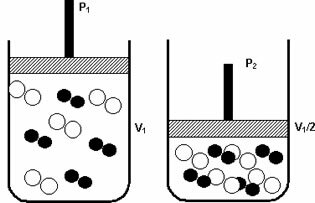
Monet kemiallisen tasapainon sisältöä koskevat harjoitukset sisältävät laskelmia, joihin sisältyy tasapainovakioiden K suhdeç (pitoisuuden suhteen) ja KP (kaasupaineiden suhteen). Jos on epäselvää, mitä nämä vakiot edustavat ja miten niiden lausekkeet kirjoitetaan jokaiselle tasapainoreaktiolle, lue teksti Kc- ja Kp-tasapainovakiot.
Näiden vakioiden suhde vahvistetaan seuraavilla kaavoilla:
Kç = KP. (R. T)n ja KP = Kç. (R. T)-n
Mutta miten nämä kaavat saavutettiin?
Tarkastellaan seuraavaa yleistä reaktiota, jossa pienet kirjaimet ovat yhtälön kertoimia ja isot kirjaimet ovat aineita (reagenssit ja tuotteet), jotka kaikki ovat kaasumaisia:
a A + b B ↔ c C + d D
Tällaista reaktiota varten tasapainovakioiden Kc ja Kp lausekkeet ovat vastaavasti:
Kç = [Ç]ç. [D]d KP = (Praça)ç. (pD)d
[THE]. [B]B (pA). (pB)B
Joten käytetään Clapeyronin yhtälöä tai kaasutilan yhtälöä:
P. V = n. A. T
p = ei. A. T
V
Aineiden pitoisuus ainemäärinä (mol / l) voidaan laskea n / V: llä. Joten voimme tehdä seuraavan korvauksen yllä olevaan kaavaan:
p = [aine]. A. T
Käyttämällä tätä kaavaa jokaiselle kyseessä olevalle reaktiolle ja reaktiotuotteille meillä on:
PTHE = [A]. A. T sB = [B]. A. T sÇ = [C]. A. T sD = [D]. A. T
[A] = __PTHE_ [B] = __PB_ [C] = __PÇ_ [D] = __PD_
A. T R. T R. T R. T
Siten voimme korvata nämä pitoisuudet yllä esitetyssä Kc-ilmentymässä:

Mutta kuten olemme nähneet, (Praça)ç. (pD)d on täsmälleen sama kuin Kp. Siksi meillä on:
(pA). (pB)B
Kç = KP. (R. T)(a + b) - (c + d)
Huomaa, että (a + b) - (c + d) on sama kuin: "reagenssien kertoimien summa - tuotteiden kertoimien summa". Joten voimme yksinkertaistaa vielä enemmän näin:
(a + b) - (c + d) = ∆n
Joten pääsemme kaavoihin, jotka liittyvät Kc: hen ja Kp:
Kç = KP. (R. T)∆ei tai K.P = Kç. (R. T)-∆ei
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Katsotaanpa joitain kemiallisen tasapainon reaktioita ja miten nämä ilmaisut määritetään heille.
Tärkeä muistiinpano:∆n sisältää vain kaasumaisessa tilassa olevien aineiden kertoimet.
N2 g) + 3 H2 g) ↔ 2 NH3 g)
Kç = KP. (R. T)(4 – 2)
Kç = KP. (R. T)2
3 O3 g) ↔ 2 O2 g)
Kç = KP. (R. T)(3 - 2)
Kç = KP. (R. T)1
Kç = KP. A. T
H2 g) + I2 g) HI 2 HI(g)
Kç = KP. (R. T)(2 – 2)
Kç = KP. (R. T)0
Kç = KP
CO(g) + EI2 g) ↔ CO2 g)+ EI(g)
Kç = KP. (R. T)(2 – 2)
Kç = KP. (R. T)0
Kç = KP
2 SO3 g) SO 2 SO2 g) + O2 g)
Kç = KP. (R. T)(2 – 3)
Kç = KP. (R. T)-1
2 EI2 g) ↔ N2O4 g)
Kç = KP. (R. T)(2 – 1)
Kç = KP. (R. T)1
Kç = KP. A. T
HCl(tässä) + AgNO3 (aq) ↔ AgCls + HNO3 (aq)
Kc = ei määritelty - ei kaasuja.
Çs + O2 g) ↔ CO2 g)
Kç = KP. (R. T)(1- 1 )
Kç = KP. (R. T)0
Kç = KP
Huomaa, että tässä tapauksessa kerroin Cs ei osallistunut.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Tasapainovakioiden Kc ja Kp suhde"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/relacao-entre-constantes-equilibrio-kc-kp.htm. Pääsy 28. kesäkuuta 2021.
Kemia

Testaa tietosi ja opi lisää tällä luettelolla kemiallisia tasapainoja koskevista ratkaisuista. Tämän materiaalin avulla pystyt ymmärtämään paremmin tasapainovakioiden (Kp, Kc ja Ki), tasapainosiirron, pH: n ja pOH: n sekä tasapainon käyttämisen ns. Puskuriliuoksissa.