Ranskalaisen kemisti Henry Louis Le Chatelierin mukaan tasapainon muutos se on tilanne, jossa kemiallinen reaktio siirtyy (eteenpäin tai taaksepäin) ulkoisen häiriön alaisena. Tämä kemian ehdottama lausunto tunnettiin nimellä Le Chatelier -periaate.
merkintä: suora reaktio on se, jossa reagoivat aineet muutetaan tuotteiksi, kun taas käänteinen reaktio on se, jossa tuotteet muutetaan reaktanteiksi.
Reaktio on tasapainossa, kun suoran reaktion nopeus on sama kuin käänteisen reaktion, ts reagoivat aineet muuttuvat tuotteiksi samalla nopeudella kuin tuotteet muuttuvat reagoiviksi.

Tasapainokemiallisen reaktion yleinen esitys
Le Chatelierin periaatteen mukaan aina kun voima vaikuttaa tasapainoreaktioon, tasapainon muutos se tapahtuu tämän häiriön poistamiseksi ja uuden tasapainotilanteen luomiseksi reaktiossa.
Häiriöt, jotka pystyvät muuttaa kemiallista tasapainoa he ovat:
→ pitoisuuden vaihtelu
kun pitoisuus aineen määrässä (mol / l tai moolina) reaktiossa osallistujan muutos (joko vähentynyt tai lisääntynyt), tasapainon muutos, kunhan osallistuja ei ole kiinteässä tilassa.
Siten Le Chatelierin periaatteen mukaan, jos pitoisuus jos osallistujaa kasvatetaan, tasapaino siirtyy kasvua vastakkaiseen suuntaan. Kuitenkin, jos pitoisuus osallistuja on vähentynyt, tasapaino siirtyy laskun suuntaan. Esimerkiksi:

Tasapainokemiallisen reaktion yleinen esitys
A-pitoisuuden lisääminen = tasapaino siirtyy oikealle
B-pitoisuuden pienentäminen = tasapaino siirtyy vasemmalle
→ Vaihtelu paine
Paineen vaihtelu vain edistää tasapainon muutos joilla on kaasumaisia komponentteja, koska kun sitä lisätään, molekyylit lisäävät törmäyksiä toistensa kanssa ja kun paine laskee, ne vähentävät törmäyksiä toistensa kanssa.
Molekyylien väliset törmäykset lisääntyvät lisääntyessä paine, koska äänenvoimakkuutta (tilaa) pienennetään vastaavasti samalla kun pienennetään paine on mukana lisääntyvä määrä.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
merkintä: Kemiallisessa tasapainossa paineenmuutoksen vaikutusta analysoitaessa otetaan huomioon reagenssien ja tuotteiden moolitilavuus, joka tilavuus liittyy reaktiokertoimiin. Alla olevassa yhtälössä reagenssitilavuus on 4 ja tuote 2.
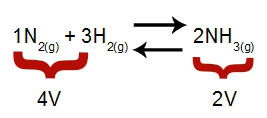
Yhtälö, joka osoittaa ammoniakin muodostumisessa olevat tilavuudet
Le Chatelierin periaatteen mukaan, jos järjestelmän paine kasvaa, järjestelmän siirtymä - tasapainossa suuremman tilavuuden suuntaan, kun taas, jos paine laskee, - saldo.

Yhtälö, joka edustaa ammoniakin muodostumisen tasapainoa
Kasvava paine = tasapaino siirtyy oikealle (koska se on puoli, jolla on vähemmän äänenvoimakkuutta).
Aleneva paine = tasapaino siirtyy vasemmalle (koska tämä on suurempi tilavuuspuoli).
→ Lämpötilan vaihtelu
Kasvu lämpötila tasapainoreaktion suosii molekyylien törmäämistä enemmän samalla kun lämpötilaa vähentää heidän levottomuuttaan ja siten niiden iskuja. Koska lämpötilan nousu suosii aina reaktiota endoterminen (joka absorboi energiaa).
Analysoitaessa lämpötilan vaikutusta tasapainoon otetaan pääasiassa huomioon reaktion AH. Jos AH on positiivinen, eteenpäin suuntautuva reaktio on endoterminen, kun taas päinvastainen on eksoterminen. Jos ΔH on negatiivinen, oikea on eksoterminen ja käänteinen endoterminen.
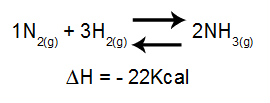
Yhtälö, joka sisältää entalpian vaihtelut ammoniakin muodostumisessa
Lämpötilan nousu = tasapaino siirtyy vasemmalle (koska tämä on endotermisen reaktion suunta, koska ΔH on negatiivinen).
Lämpötilan lasku = tasapaino siirtyy oikealle (koska tämä on eksotermisen reaktion suunta, koska ΔH on negatiivinen).
Minun luona. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Mikä on tasapainosiirtymä?"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-deslocamento-equilibrio.htm. Pääsy 28. kesäkuuta 2021.