Kuna oktetireeglil on erandeid, siis kuidas me saame teada aatomite õiget paigutust molekuli moodustamisel?
Seda saab teha iga struktuuri ametliku koormuse arvutamise teel. Nullile lähim ametlik laeng on tegeliku eksistentsi kõige suurema tõenäosusega. Pange tähele, et see on nullile lähemal, seega ei pea see olema null.
Ametlik laenguvalem (Cfo) é:
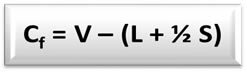
V = vaba aatomi valentselektronide arv;
L = elektronide arv, mis esinevad struktuuris aatomi isoleeritud (mittesiduvates) paarides;
S = aatomiga struktuuris jagatud elektronide arv.
Et mõista, kuidas see juhtub, kujutage ette, et tahame teada, milline on Lewise elektrooniline struktuur SO-molekuli jaoks.2. Aatomite vahel on meil kaks võimalust:
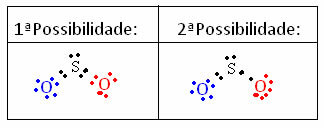
Arvutatakse kõigi struktuurides osalevate aatomite ametlik tasu. Vaata:
1. võimalus:
Väävel (S): Hapnik (O) Hapnik (O)
Çf (S) = 6 – (2 + ½ 8) Çf (S) = 6 – (4 + ½ 4) Çf (S) = 6 – (4 + ½ 4)
Çf (S) =0 Çf (S) =0 Çf (S) =0
Ärge lõpetage kohe... Peale reklaami on veel;)
2. võimalus:
Väävel (S): Hapnik (O) Hapnik (O)
Çf (S) = 6 – (2 + ½ 6) Çf (S) = 6 – (6 + ½ 2) Çf (S) = 6 – (4 + ½ 4)
Çf (S) = +1Çf (S) = -1 Çf (S) =0
Saadud tulemuste põhjal võime märkida, et 1. struktuur on kõige suurema tõenäosusega reaalne eksisteerimine. Niisiis, me teame, et see ei järgi oktetti reeglit, kuid väävel on laiendanud oma valentskesta, püsides stabiilsena 10 elektroniga.
See reegel kehtib ka õige ioonide paigutuse leidmiseks.
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Ametlik koormuse arvutamine"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm. Juurdepääs 28. juunil 2021.