1786. aastal lahkas Itaalia anatoom Luigi Galvani (1737–1798) oma laual konna, millel oli elektrostaatiline masin. Galvani vaatas looma lihaseid kokku tõmbumas, kui tema abiline puudutas kogemata skalpelli otsa konna reie sisemisele närvile. Teisisõnu, see juhtus siis, kui konna kudesid puudutasid kaks erinevat metalli.
Galvani hakkas sellest hetkest kaitsma teooriat, mis üritas seda fakti seletada: „loomade elektri” teooriat. Galvani sõnul olid metallid vaid elektrijuhid, mis tegelikkuses sisalduksid konna lihastes.
Kuid tema teooria oli vale ja seda nägi Itaalia füüsik Alessandro Volta (1745–1827), kes viis läbi mitmeid katseid ja märkasin, et kui plaat ja traat olid valmistatud samast metallist, ei ilmnenud krampe, mis näitas, et elekter. Seega jätkas ta selle (õige) kontseptsiooni kaitsmist, et elekter ei pärine konna lihastest, vaid metallidest ja et looma kuded juhivad seda elektrit.
Volta õigsuse tõestamiseks tegi Volta elektrolüütilise lahusega moodustatud vooluahela ehk ioonidega lahuse lahustunud, mida ta nimetas märjaks või teise klassi juhiks, mis oli kokkupuutes kahe elektroodiga metallik. Neid viimaseid nimetas Alessandro Volta kuivadeks või esimese klassi dirigentideks.
Ta tegi seda, asetades märja juhi (mis oli soolalahuse vesilahus) kahe kuiva juhi (mis olid juhtme abil ühendatud metallid) vahele. Sel hetkel täheldas ta, et elektrivool ärkab. Samuti sai ta aru, et sõltuvalt kasutatavatest metallidest võib vooluhulk olla suurem või väiksem. Seega võime tunnistada, et idee sellest, mis on hunnik, oli Volta juba aru saanud ja seletanud.
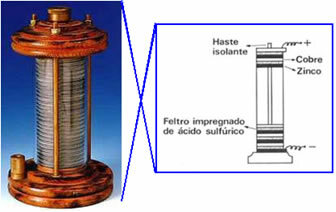
Aastal 1800 lõi Volta esimese elektrielemendi, mida hakati nimetama tagumine kuhi, galvaaniline vaia või voltaallakk ja ikkagi, "roosikrantsi". Selle kuhi skeem on toodud allpool: ta asetas väävelhappelahuses leotatud vildiketta peale vaseketta ja lõpuks tsingiketta; ja nii edasi, virnastades need sarjad suurde veergu. Vasel, vildil ja tsinkil oli keskel auk ja need olid keermestatud horisontaalse varda külge, ühendades seeläbi juhtme abil.
Ärge lõpetage kohe... Peale reklaami on veel;)
See katse põhjustas teadusmaailmas ja pärast seda kõigis seadmetes, mis toodavad elektrit protsessidest, murranguid kemikaale (see tähendab, et keemilise energia tootmine elektrienergiaks) hakati nimetama volttelementideks, galvaanielementideks või lihtsalt patareid.
Volta tegi sama katse erinevate metallide ja elektrolüütide lahustega, näiteks soolvees leotatud flanellketastega eraldatud hõbe- ja tsinkketastega. Ta näitas seda avastust isegi Napoleon Bonaparte'ile, nagu on näha alloleval joonisel, Pariisi Teaduste Akadeemias.

Alessandro Volta demonstreerib Napoleonile oma avastust
Teine Volta eksperiment patareidega oli prillide kroon, kuhu ta asetas kaks juhtmetega ühendatud, kuid elektrolüüdilahustega eraldatud erinevat metalli plaati.
Praegu teame, et rakus, nagu Volta loodud, juhtub see, et elektrit voolab poolusest. negatiivne, mida nimetatakse anoodiks, mis oksüdeerub, kaotades elektronid positiivsesse poolusesse, mida nimetatakse katoodiks, mis vähendab, elektronid.
Neid vesilahuses valmistatud akusid ei kasutata tänapäeval eriti palju; lihtsalt teadusuuringute osas, kuid need olid põhimõte, mis arendas välja tänapäevased patareid, mida me täna patareidena tunneme kuiv ja neid on palju otstarbekam kasutada ja kanda, samuti pakkuda rahuldavat elektrivoolu palju enama jaoks. aeg.
Autor Jennifer Fogaça
Lõpetanud keemia


