Molekulide polaarsus on väga oluline aspekt, kuna ainete omadused määratakse muude tegurite hulgas ka asjaolust, et nende molekulid on polaarsed või mittepolaarsed.
Molekuli polaarsuse saab määrata meetodi abil Dipoolmoment või Tulemuseks olev dipoolmoment, mille sümbol on 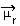 . Kui me räägime lihtsalt molekulis iga sideme dipoolmomentist, siis on sümbol kreeka täht mi (µ).
. Kui me räägime lihtsalt molekulis iga sideme dipoolmomentist, siis on sümbol kreeka täht mi (µ).

Molekul on mittepolaarne, kui dipoolmoment on võrdne nulliga, kuid kui see on nullist erinev, tähendab see, et see on polaarne.

Selle tekkiva dipoolmomendi määramisel tuleb arvestada kahe olulise asjaga. Vaatame, mis need on:
1) elektronegatiivsuse erinevus reaktsioonis osalevate elementide aatomite vahel. Näiteks on HF-molekulil märkimisväärne erinevus elektronegatiivsuses, kuna fluor tõmbab sidemes olevate elektronide paari palju rohkem kui vesinik. Seega ei ole laengute jaotus sümmeetriline, elektriliste dipoolidega.
Seda dipooli esindab vektor, mis on suunatud otsa poole, mis koondab kõige rohkem elektrone, see tähendab kõige vähem elektronegatiivsest aatomist. Niisiis, antud juhul on vektor, mis on ainus, saadud vektor, nagu allpool näidatud:
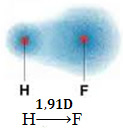
Pange tähele, et vektori väärtus on sama kui dipoolmoment, mis on antud debye ühikus (D = 3,33. 10-30 kulon. metroo). Kuna dipoolmoment on nullist erinev, on molekul ja side polaarne.
Ärge lõpetage kohe... Peale reklaami on veel;)
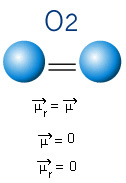
Allpool olevas molekulis on meil ka ainult kahe aatomiga molekul, kuid antud juhul vastab see lihtsale ainele, see tähendab, et selle moodustab ainult ühte tüüpi element. Seetõttu puudub elektronegatiivsuse erinevus; aatomid tõmbavad ligi ka elektronid, mis on sümmeetriliselt jaotunud. Saadud dipoolmoment on võrdne nulliga, nii et nii side kui ka molekul on apolaarne.
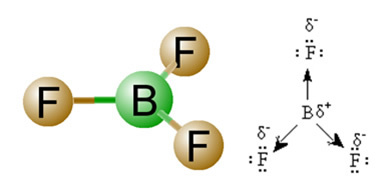
2) Molekuligeomeetria, see tähendab vektorite ruumiline paigutus. BF molekul3 sellel on kolm polaarsidet, milles fluor on kõige elektronegatiivsem, seega on vektorid suunatud sellele. Kuna aatomite ruumiline paigutus on kolmnurkne tasapinnaline, siis muudab see elektronide sümmeetrilise jaotuse ümber keskaatomi. Seega on tulemus see, et need kolm vektorit tühistavad üksteise ja dipoolmoment on võrdne nulliga. Seega BF molekul3 é vabandama.
Veemolekulil on kaks vektorit, kuid selle ruumiline geomeetria ei ole tasane, vaid V-kujuline. Järgmisel joonisel pange tähele, et nii ei tühista nende vektorid üksteist, elektronid jaotuvad asümmeetriliselt ja kontsentreeruvad kõige rohkem elektronegatiivsesse aatomisse, milleks on hapnik. Seega erineb dipoolmoment nullist ja veemolekul polaarne:
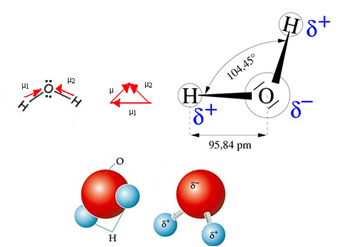
Autor Jennifer Fogaça
Lõpetanud keemia