Valdav osa looduses, meie ühiskonnas ja kehas leiduvatest materjalidest ei ole puhtad ained, vaid tegelikult segud kahest või enamast aineid.
Kuigi me nimetame mineraalvett enamasti ainult „veeks“, ei sisalda see tegelikkuses ainult puhast ainet H2O, sest see on protsessi tulemus, kus vihmavesi tungib mulda ja läbib erinevaid kive.
Niisiis, nagu nimigi ütleb, on sellel lisaks veele ka mitu lahustunud mineraali. Kui olete huvitatud mineraalvee märgistuse kontrollimisest, näete, et selle koostis on olemas keemiast strontsiumsulfaadid, kaltsium, naatrium, kaalium, naatriumvesinikkarbonaat, naatriumfluoriid teised.
Meelekaart: segud
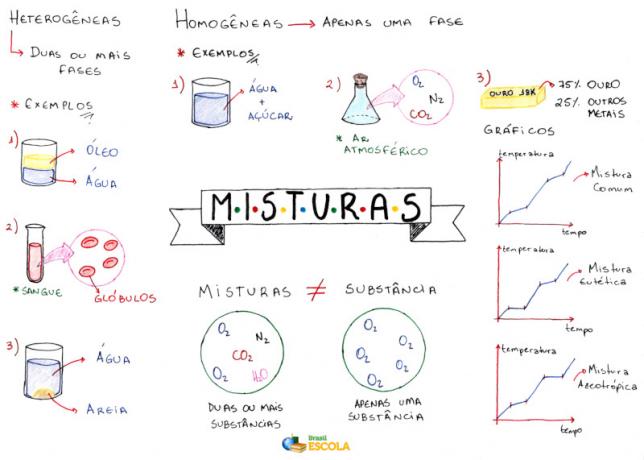
* Mõttekaardi allalaadimiseks PDF-failina Kliki siia!
Kuidas on võimalik ainet segust eristada?
Allpool näidatud destilleeritud vesi on puhas aine, mis sisaldab ainult H2O:

Laboris kasutatav destilleeritud vesi
Visuaalselt näeb see välja täpselt nagu vee ja soola segu; neid saab aga segude määratlusest eristada. Vaata:
→ Segud on materjalid, mille füüsikalised omadused pole konstantsed, vaid varieeruvad teatud temperatuuril ja rõhul.
Niisiis, lihtsalt mõõta füüsikalised omadusednagu sulamis- ja keemistemperatuurid ning tihedus. Kui need on konstantsed ja täpselt määratletud, on see a puhas aine (destilleeritud vee korral temperatuuril 4 ° C on selle tihedus 1,0 g / cm33 ja merepinnal on sulamis- ja keemistemperatuur vastavalt 0 ° C ja 100 ° C).
Ärge lõpetage kohe... Peale reklaami on veel;)
Kui esitatakse variatsioone, on see segu. Kui keedate vee ja soola segu keemistemperatuuri kontrollimiseks, näete seda vedelal olekul üleminekul gaas, ei püsi temperatuur konstantsena nagu destilleeritud veega, mis püsib 100 ° C juures, kuni kogu vedelik pöördub aur.
Nüüd on segud et nende segude teadmiseks pole vaja isegi nende füüsikalisi omadusi kindlaks teha, vaadake lihtsalt, nagu on järgmine vee ja õli segu:

Vee ja õli moodustunud segu
See näitab, et segusid on erinevat tüüpi, mida saab liigitada homogeenne ja heterogeenne. Vaadake kõiki:
Homogeensed segud:
Need on ühtse välimusega, ühefaasilised (üksik faas). Näited:
soolalahus (0,9 g naatriumkloriidi 100 ml vees);
soolvees (36 g sooli, nagu naatriumkloriid, magneesiumkloriid, kaaliumjodaat, anti-niisutavad ained ja 100 ml vett);
hüdraatunud alkohol (etanool ja vesi);
õhk (78% gaasilist lämmastikku, 20% hapnikku, 2% muid gaase ja veeauru);
teras (metallisulam, mis on moodustatud 98,5% rauast ja 1,5% süsinikust).

Soolalahus, teras ja formaldehüüd, näited homogeensetest segudest
Eespool toodud näited näitavad seda homogeensed segud need võivad olla tahkes, vedelas või gaasilises olekus. Neid homogeenseid segusid nimetatakse lahendusi ja neid ei saa lahutada füüsikaliste meetoditega, vaid ainult keemiliste meetoditega. Näiteks alkoholi eraldamiseks veest on vaja läbi viia protsess destilleerimine, sest a tsentrifuug või filtreerimine see ei teeks.
Lisaks on oluline rõhutada, et need peavadki olema homogeenne isegi ultramikroskoobi all vaadates. Näiteks palja silmaga võivad piim ja veri tunduda homogeensed, kuid ultramikroskoobi all näeme, et tegelikult on need heterogeenne. Pärast ultracentrifuugi paigutamist vaadake vere kujutist ultramikroskoobi all ja selle eraldi faase:
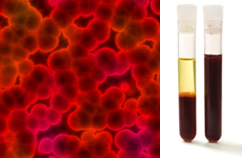
Mikroskoopiline pilt ja vere faasid
Heterogeensed segud:
Kas need, millel on rohkem kui üks faas. Näited: vesi ja õli, vesi ja liiv, jää ja vesi, graniit, vesi ja raud, vees lahustumatu sool jne.
Komponendid heterogeensed segud need ilmnevad enamasti erinevates füüsikalistes olekutes ja neid saab füüsikaliste meetoditega eraldada. Näiteks võib tuua kohvi valmistamise ja tahke aine filtreerimise, eraldades selle vedelikust.
Kuid seda ei juhtu alati, nagu näitab õli ja vesi, mis vaatamata mõlemale vedelikule ei lahustu erinevate selle molekulide polaarsused.
Vaimne kaart Ema Victor Ricardo Ferreira
Keemiaõpetaja
Autor Jennifer Fogaça
Lõpetanud keemia


