Halogeenimisreaktsioonid on orgaanilise asendusreaktsiooni tüüp, see tähendab, et a aatom või aatomirühmad asendatakse teise molekuli aatomite või aatomirühmadega orgaaniline.
Üldiselt toimub seda tüüpi reaktsioon alkaanide ja aromaatsete süsivesinikega (benseen ja selle derivaadid).
Halogeenimist nimetatakse nii, kuna see toimub halogeenide lihtsate ainetega: F2, Cl2, br2 Hei2. Kõige tavalisem neist on siiski kloorimine (Cl2) ja broomimine (Br2), kuna fluor on väga reaktiivne ja selle reaktsioonid on plahvatusohtlikud ja neid on raske kontrollida, hävitades isegi orgaanilisi aineid:
CH4 g) + 2 F2 g) → Cs) + 4HFg)
Reaktsioonid joodiga on äärmiselt aeglased.
Allpool on toodud halogeenimise peamised tüübid ja mõned näited:
1. Halogeenimine alkaanidega: Kuna alkaanid on halvasti reageerivad, toimuvad nende halogeenimisreaktsioonid ainult päikesevalguse (λ), ultraviolettvalguse või tugeva kuumutamise korral. Seda tüüpi reaktsioone tehakse alküülhalogeniidi saamiseks.
Näide: metaani monokloorimine:
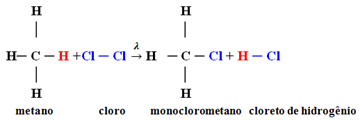
Sel juhul tekkis see metaani vesinikuaatomist (CH4) asendatakse klooriaatomiga, saades monoklorometaani. Kui kloori oli liiga palju, võib see reaktsioon jätkuda, asendades kõik metaanis olevad vesinikud.
1.1. Halogeenimine enam kui 3 süsinikuga alkaanides: Kui reageerival alkaanil on vähemalt 3 süsinikuaatomit, jõuame lõpuks erinevate asendatud ühendite segusse. Vaadake allpool toodud metüülbutaanmonokloorimise näidet:
Ärge lõpetage kohe... Peale reklaami on veel;)
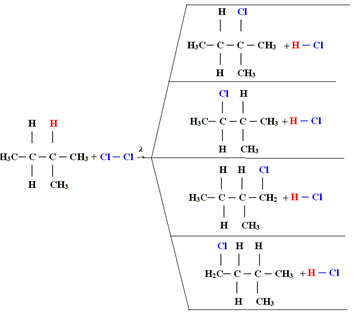
Iga ühendi kogus on proportsionaalne järgmise kerguse järjekorraga, millega vesinik molekuli eraldub:

Seega on ülaltoodud juhul suurim kogus 2-metüül-2-klorobutaani ja väikseim 2-metüül-1-klorobutaan.
2. Benseeni halogeenimine: Benseen ei reageeri tavaliselt kloori ega broomiga. Kui aga katalüsaatorina kasutatakse Lewise hapet (tavaliselt kasutatakse FeCl3, FeBr3 või AlCl3, kõik veevabas vormis), reageerib benseen halogeenimisreaktsioonis kergesti.
Kloriidi ja raudbromiidi saab lihtsalt segule raua lisamisega ja sel viisil reageerib see halogeeniga ja tekitab Lewise happe:
2 Fe + 3 Br2 → 2 FeBr3
Vaadake benseeni halogeenimise näidet ja selle mehhanismi:
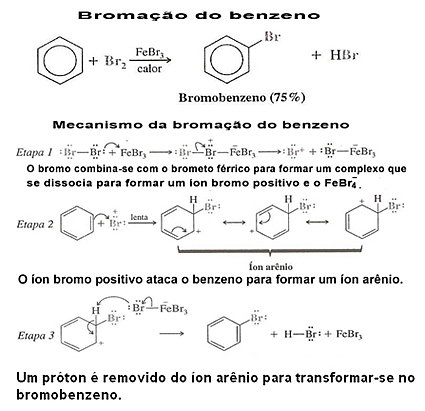
3. Benseeni derivaatide halogeenimine:Sellistel juhtudel juhib asendust aromaatse tuuma külge kinnitatud asendaja või funktsionaalne rühm. Kuidas see juhtub, lugege tekste "Radikaalide juhtimine benseeniringis"ja"Meta- ja orto-lavastajate radikaalide elektroonilised efektid”.
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Orgaanilised halogeenimisreaktsioonid"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm. Juurdepääs 28. juunil 2021.