THE nihoonium, aatomnumber 113 ja sümbol Nh on perioodilise tabeli rühma 13 kuuluv keemiline element. Lisaks on see üliraske element, mida looduses ei leidu. Seega saab seda saada ainult kunstlikult, tuumasünteesi reaktsioonide kaudu. Nihooniumi keemilised omadused on endiselt ebaselged, kuid oletatakse, et see käitub mõnel juhul sarnaselt oma kergema kolleegi talliumiga.
Nihoonium saadi algselt sulatamise teel 70Zn koos 209Bi Jaapanis Rikeni Instituudis 2003. aastal. Kuigi ka Venemaa ja Ameerika teadlased palusid end tunnistada elemendi 113 avastajateks, tunnustas IUPAC Jaapani teadlasi. Nimi viitab sõnale Nihon, nagu jaapanlased oma kodumaad nimetavad.
Loe ka: Gallium — teine keemiline element, mis kuulub perioodilise tabeli rühma 13
Selle artikli teemad
- 1 - Kokkuvõte nihooniumi kohta
- 2 - Nihooniumi omadused
- 3 - nihooniumi omadused
- 4 - nihooniumi saamine
- 5 – Nihônio ajalugu
- 6 - Lahendati harjutusi nihooniumi kohta
kokkuvõte nihooniumi kohta
See on sünteetiline keemiline element, mis asub rühmas 13 Perioodilisustabel.
Selle tootmine algas 2003. aastal Jaapanis Rikeni Instituudis.
See moodustab 2015. aastal perioodilisustabelisse viimati lisatud elementide rühma.
Tema uuringud on veel väga hiljutised, kuid mõned püüavad seda seostada teiste 13. rühma elementidega, näiteks talliumiga.
Selle tootmine on Tuumasünteesi, kasutades isotoope 70Zn ja selle aatomid 209Bi.
Ära nüüd lõpeta... Pärast kuulutust on rohkem ;)
Nihooniumi omadused
Sümbol: ei
Aatomnumber: 113
Aatommass: vahemikus 278–286 c.u. (mitteametlik, Iupac)
Elektrooniline konfiguratsioon: [Rn] 7s2 5f14 6d10 7p1
Kõige stabiilsem isotoop:286Nh (9,5 sekundit pool elu, mis võib suureneda 6,3 sekundi võrra või väheneda 2,7 sekundi võrra)
Keemiline seeria: rühm 13, ülirasked elemendid
nihooniumi omadused
Nihoonium, sümbol Nh ja aatomnumber 113, oli üks viimaseid perioodilise tabeli elemente. Selle ametlikuks muutis 30. detsembril 2015 Rahvusvaheline Puhta ja Rakenduskeemia Liit (IUPAC), samas kui selle nimi tehti ametlikuks alles 2016. aasta keskel.
Selle perioodilise tabeli piirkonna elemendid on väga ebastabiilsed, mis tähendab, et neid ei leidu looduses. Seega läbiksid need väidetava olemasolu korral peaaegu koheselt radioaktiivse lagunemise – tuumaosakeste, nagu α ja β, emissiooni, et saavutada suurem stabiilsus.
Kui nad aga kiirgavad tuumaosakesi, läbivad nad tuumatransmutatsiooni, see tähendab, et neist saab uus keemiline element. Seega tuleb laboris toota üliraskeid elemente, nagu Nh, mis muudab selle a sünteetiline keemiline element.
Nh, nagu ka teised ülirasked elemendid, on mõjutatud relativistlikud efektid — lihtsal viisil relatiivsusest tulenevad kaugused vaadeldavast oodatuni. Nii tõid relativistliku efekti tagajärgi simuleerivad teoreetilise valdkonna matemaatilised uuringud välja, et nihoonium võiks kvartsiga nõrgalt suhelda, kuid omama hea adsorptsioon kullast, nagu selle kergem vaste tallium (Tl).
Esialgsed teoreetilised uuringud näitasid ka volatiilsus alates Nh. Mis puudutab adsorptsiooni kvartsile, siis tallium moodustab kergesti näiteks TlOH-d ja nihoonium kahtlustatakse sedasama.
Isegi nii, kuidas uuringud on veel väga esialgsed ja värsked, on suur osa sellest, mis on toodetud, aruteluks avatud ja nihooniumi füüsikalis-keemilisi omadusi on raske täpselt määrata.
Nihooniumi saamine
Element 113 on kuni tänaseni saadud kahel viisil: läbi külmsünteesi reaktsioonidtsingi (Zn, Z = 30) sulandumisel vismutiga (Bi, Z = 83) ja ka läbi elemendi 115 alfa lagunemine.
Esimeses näites on tsink kiirendatakse 10%-ni valguse kiirus, et ületada kahe tuuma tõukejõud. Seejärel toodetakse isotoop 279Nh, mis lõpuks kiirgab neutroni ja tekitab 278Nh.

Umbes 34 millisekundilise poolestusajaga isotoop 278Nh läbib kuus alfalagunemist (alfaosakeste emissioon) elemendiks mendelevium (Md).
Teisel juhul tekib element 113 elemendi 115 (praegu tuntud kui muskoviumi) alfa-lagunemisest pärast selle sünteesimist. Üks võimalus on ioonide kuumsünteesi reaktsioon 48Ca isotoopidega 243ah, toodab 288Mc ja seejärel alfa lagunemise teel 284Nh, mis jätkab alfalagunemist.
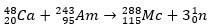
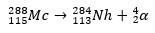
Vaata ka: Hassium – kõige raskem sünteetiline keemiline element, mille omadusi on analüüsitud
nihooniumi ajalugu
Elemendi 113 otsinguid alustati 2003. aastal. Jaapani teadlased Rikeni Instituudist kiirendasid isotoope 70Zn 10% valguse kiirusest, et põrkaks kokku 209Bi, termotuumasünteesi reaktsiooni kaudu. Seega õnnestus neil toota seda, mida me praegu tunneme 278Nh.
See oli aga alles 2012. aastal Jaapani teadlased suutsid tuvastada täieliku alfalagunemise seeria elemendist 113, võttes avastuse taotlemiseks ühendust IUPAC-iga.
Samaaegselt Jaapani jõupingutustega tegid Vene teadlased Juri Oganessiani juhtimisel koostööd Ameerika teadlased jõudsid elemendi 113 tuvastamiseni ka elemendi alfalagunemise kaudu 115. Sellised katsed panid Venemaa ja Ameerika teadlased võistlema ka elemendi 113 äratundmise pärast.

Kuid IUPAC leidis, et Rikeni instituudi tõendid on kindlamad ja andis seega jaapanlastele õiguse nimetada elementi 113. Valitud nimi oli nihônio, sümbol Nh, viidates riigile Jaapan. Jaapanlased on kirjutanud sõna Jaapan, kasutades kahte hiina tähemärki, mis tähendavad "tõusva päikese maad" ja mida loetakse kui Nihon või Nippon.
Nimetus nihoonium valiti ka seetõttu, et 1908. aastal avaldas Jaapani keemik Masataka Ogawa, et oli avastanud elemendi 43, pannes selle jaapanikeelseks, sümboliks Np (mis tänapäeval kuulub neptuuniumile, Z = 93). Hiljem aga tõestati, et element 43 oli ebastabiilne, seda looduses ei leitud ja sünteesiti alles 1937. aastal, saades nimetuse tehneetsium (Tc).
Nii kadusid jaapanlased perioodilisest tabelist. Kuid aastaid hiljem tõestati, et tegelikult oli Ogawa avastanud elemendi 75 (praegu tuntud kui reenium). Selleks ajaks oli aga element reenium juba 1925. aastal ametlikult avastatud ja ristitud.
Lahendas harjutusi nihooniumil
küsimus 1
Nihoonium, sümbol Nh ja aatomnumber 113, on keemiline element, mida lühikese poolestusaja tõttu looduses ei leidu. Kõige vastupidavam neist, 286Nh, on umbes 9,5 sekundit. Teades, et poolestusaeg on aeg, mis kulub liikide arvukuse poole võrra vähenemiseks, mitu sekundit kulub selleks, et ülaltoodud isotoobi kogus oleks 1/16 kogusest esialgne?
A) 9.5
B) 19
C) 28,5
D) 38
E) 47,5
Resolutsioon:
Alternatiiv D
Iga 9,5 sekundi järel väheneb isotoobi kogus poole võrra. Seega on 9,5 sekundi pärast selle kogus pool esialgsest summast. Veel 9,5 sekundit, kokku 19 sekundit, väheneb summa taas poole võrra, jõudes 1/4ni esialgsest.
28,5 sekundi pärast, pärast teist poolväärtusaega, väheneb kogus uuesti poole võrra, ulatudes 1/8 esialgsest kogusest. Lõpuks, 38 sekundi pärast, väheneb summa jälle poole võrra, jõudes 1/16-ni esialgsest summast, nagu avalduses nõutud. Seega kuluv aeg on 38 sekundit.
küsimus 2
2003. aastal hakati Jaapanis Rikeni Instituudis otsima elementi 113. Sel ajal suutsid teadlased toota 278Nh tsingi ja vismuti aatomite ühinemise kaudu.
Mitu neutronit on nimetatud isotoobis?
A) 113
B) 278
C) 391
D) 170
E) 165
Resolutsioon:
Alternatiiv E
Arv neutronid saab arvutada järgmiselt:
A = Z + n
kus A on arv pasta aatomiline, Z on aatomarv ja n on neutronite arv. Väärtuste asendamisel on meil:
278 = 113 + n
n = 278-113
n = 165
Autor Stefano Araújo Novais
Keemia õpetaja
