- Neutraalne keskkond:
Söödet loetakse neutraalseks, kui selle hüdrooniumiioonide kontsentratsioon mol/l on sama (H3O+) ja hüdroksiid (OH-).
Näide neutraalsest keskkonnast, mis toimib isegi muude lahuste standardina, on puhas, destilleeritud vesi, mille temperatuur on 25 °C. Sellel temperatuuril on see täpselt 1. 10-7 mol/l mõlemat iooni. Seega on teie ioonne toode (Kw) võrdub 10-ga-14 (mol/l)2:
Kw = [H3O+]. [oh-]
Kw = (1. 10-7 mol/L). (1. 10-7 mol/L) = 10-14 (mol/l)2
pH ja pOH on toodud allpool:
pH= - log [H3O+] pOH= -log[OH-]
pH= - log 1. 10-7 pOH= - log 1. 10-7
pH = 7pOH = 7
See näitab meile, et neutraalses lahenduses pH on võrdne pOH-ga.
- Happeline keskkond:
Happelises keskkonnas H-ioonide kontsentratsioon3O+ on suurem kui OH-ioonidel-.
Sellise lahenduse saab saavutada väikese osa H-ioonide lisamisega3O+näiteks happe abil.
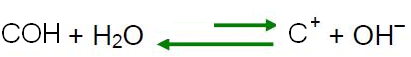
Le Chatelier' põhimõtte kohaselt, kui tasakaalus olevas süsteemis tekitatakse häire, kipub see end ümber kohandama, et selle jõu mõjusid vähendada. See tähendab, et kui veele lisada hapet, siis H-ioonid
3O+ neid on üle ja tasakaal nihkub vastupidises reaktsiooni suunas, vasakule. Nii et need liigsed ioonid reageerivad OH-ioonidega-. Seega OH ioonide kontsentratsioon- väheneb ja lahus muutub happeliseks.Ära nüüd lõpeta... Peale reklaami on veel midagi ;)

Ioonne korrutis (Kw) on alati võrdne 10-ga-14, vaid H-ioonide kontsentratsioon3O+ on suurem kui OH ioonide kontsentratsioon-1. Seetõttu on pH happelises keskkonnas suurem kui pOH, kuid selle summa on alati 14.
Samuti, mida suurem on H-ioonide kontsentratsioon3O+, seda suurem on pH väärtus. Toatemperatuuril (25°C), pH < 7 ja pOH > 7.

- Põhilised vahendid:
Aluselises keskkonnas OH ioonide kontsentratsioon- on suurem kui H-ioonide oma3O+.
Kui lisame veele aluse, tähendab see, et lisame OH ioone.- ja nagu eelmises punktis selgitatud, Le Chatelier' põhimõttel, reaktsiooni tasakaal Vee iseioniseerumine liigub vastupidises suunas, liigne ioon reageerib sellega H ioonid3O+, vähendades teie kontsentratsiooni ja muutes lahuse aluseliseks.
Sel juhul on pOH suurem kui pH. Toatemperatuuril (25°C), pH > 7 ja pOH < 7.

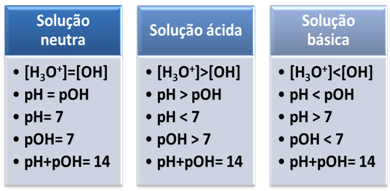
Lühidalt:
Autor Jennifer Fogaça
Lõpetanud keemia eriala
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Neutraalne, happeline ja aluseline sööde"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/meios-neutro-acido-basico.htm. Sissepääs 27. juulil 2021.


