Puhas aine moodustub ühte tüüpi keemilistest liikidest, see tähendab, et selle koostis ja omadused on fikseeritud. Mix sisaldab mitut tüüpi komponente, seega on selle korraldus erinev.
Seega saame puhast ainet segust eristada ainult siis, kui teame selle koostist.
Kui võrrelda klaasi vett ja klaasi lahustunud suhkrut, ei märka meie silmad mingit erinevust. Kui aga neelame kahe klaasi sisu sisse, märkame, et üks on puhas aine ja teine segu.
puhtad ained
Puhas aine on ainult ühe keemilise liigi kogum, see tähendab, et seda ei segata teistega.
Kasutame näiteks vett. Vesi (H2O) on tunnustatud oma omaduste poolest ja selle materjali spetsiifilised omadused aitavad meil seda tuvastada. Peamine vee omadused nemad on:
| Tihedus | 1,00 g / cm3 |
|---|---|
| Sulandumispunkt | 0 ° C |
| Keemispunkt | 100 ° C |
Kui materjalil on kogu ulatuses fikseeritud ja muutumatud omadused, ütleme, et see on a puhas aine.
Kui paneme lauasoola, naatriumkloriidi (NaCl) klaasi vette ja segame, toimub muutus.

Tulemuseks on toote keskmise tihedusega vesi ja sool. Seda seetõttu, et vesi pole enam puhas aine ja sellest on saanud a Sega.
Kui proovite seda segu külmutada, märkate, et sulamistemperatuur jääb alla 0 ° C ja nii ka see segu ei keeda 100 ° C juures, selle aurustamiseks on vaja rohkem soojust toote.
Puhtad lihtsad ja liitained
Puhtad ained klassifitseeritakse lihtsateks, kui nende koostises on ainult ühe keemilise elemendi aatomid.
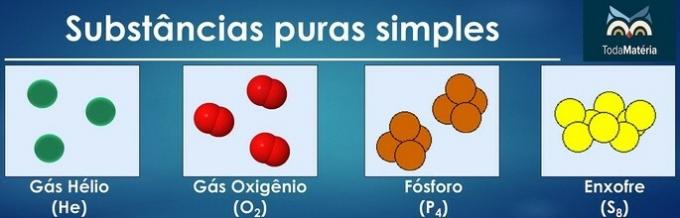
Kahe või enama keemilise elemendi aatomite paigutus moodustab puhtaid liitühendeid.

Segud
Segu vastab kahe või enama puhta aine ühendamisele, mida nimetatakse komponentideks.
Erinevalt puhastest ainetest ei ole selle omadused fikseeritud, kuna need sõltuvad komponentide osast segus.
Vaadake, kuidas tihedus, füüsikaline omadus, erineb veega segatud soola kogusest.
| Soola osakaal protsentides kogu segu mass |
Segu tihedus (g / cm3) temperatuuril 20 ° C |
|---|---|
| 1 | 1,005 |
| 8 | 1,056 |
| 12 | 1,086 |
| 16 | 1,116 |
| 26 | 1,197 |
Allikas: FURNISS, B. S. jt. Vogeli praktilise orgaanilise keemia õpik. 4. toim. London: Longman, 1987. P. 1.312.
Seetõttu on vee ja soola lisamine mis tahes vahekorras muutuva tihedusega ja seetõttu ei saa me segu klassifitseerida ei vee ega soolana.
Homogeensed ja heterogeensed segud
Homogeensed segud on need, mis sisaldavad komponente ainult ühes faasis ja seetõttu kõigis punktides samad omadused.

Kui tajume visuaalselt rohkem kui ühte faasi, klassifitseeritakse segu heterogeenseks.

Kokkuvõte puhaste ainete ja segude kohta
| Puhtad ained ja segud | |
|---|---|
|
homogeenne süsteem (ainult üks faas) |
puhas aine (üks komponent) |
|
homogeenne segu (samas faasis rohkem kui üks komponent) | |
|
heterogeenne süsteem (rohkem kui üks faas) |
puhas aine (komponent erinevates füüsikalistes olekutes) |
|
heterogeenne segu (rohkem kui üks komponent rohkem kui ühes faasis) |
Lisateabe saamiseks kontrollige kindlasti neid tekste:
- Aatomid
- Keemilised elemendid
- Segude eraldamine
Harjutused koos kommenteeritud tagasisidega
1. (UFMG) Puhta aine X proovil olid mõned selle omadused kindlaks määratud. Kõigil alternatiividel on omadused, mis on selle aine tuvastamiseks kasulikud, välja arvatud:
a) tihedus.
b) proovi mass.
c) vees lahustuvus.
d) keemistemperatuur.
e) sulamistemperatuur.
Vale alternatiiv: b) proovi mass.
a) ÕIGE. Tihedus on aine kogus antud mahus. Materjalispetsiifilise omadusena on see kasulik aine tuvastamiseks.
b) VALE. Mass on aine kogus kehas. Kuna see omadus kehtib mis tahes aine suhtes, olenemata selle ehitusest, ei ole seda võimalik aine tuvastamiseks kasutada.
c) ÕIGE. Lahustuvus on aine võime antud vedelikus lahustuda või mitte. Materjalispetsiifilise omadusena on see kasulik aine tuvastamiseks.
d) ÕIGE. Keemistemperatuur vastab vedeliku olekust gaasilise oleku temperatuurile. Materjalispetsiifilise omadusena on see kasulik aine tuvastamiseks.
e) ÕIGE. Sulamistemperatuur vastab vedeliku tahke oleku muutumise temperatuurile. Materjalispetsiifilise omadusena on see kasulik aine tuvastamiseks.
2. (Vunesp) Allpool on reprodutseeritud mineraalvee pudeli silt.
| Tõenäoline keemiline koostis: |
|---|
| Kaltsiumsulfaat 0,0038 mg / l |
| Kaltsiumbikarbonaat 0,0167 mg / l |
Selle teabe põhjal saame klassifitseerida mineraalvee järgmiselt:
a) puhas aine.
b) lihtne aine.
c) heterogeenne segu.
d) homogeenne segu.
e) kolloidne suspensioon.
Õige alternatiiv: d) homogeenne segu.
a) VALE. Vesi oleks puhas, kui selle koostises oleks ainult H-molekule2O.
b) VALE. Lihtne aine koosneb ainult ühe keemilise elemendi aatomitest. Samuti pole puhas vesi lihtne aine, kuna selle moodustavad vesiniku ja hapniku aatomid (H2O) see on klassifitseeritud liitmaterjaliks.
c) VALE. Heterogeensel segul on rohkem kui üks faas, sel juhul saame jälgida ainult vett.
d) ÕIGE. Kuna sellel on ainult üks faas, on süsteem homogeenne. Veepudelit vaadates näeme ainult vedelikku, kuna kaltsiumsulfaat ja kaltsiumbikarbonaadi ühendid lahustuvad vees ja on seetõttu lahustunud.
e) VALE. Kolloidne suspensioon on heterogeenne segu, mille komponente eristatakse mikroskoobi abil.
3. (UCDB) Keemialaboris valmistati järgmised segud:
Mina vesi / bensiin
II. vesi / sool
III. vesi / liiv
IV. bensiin / sool
V. bensiin / liiv
Millised neist segudest on homogeensed?
a) Puudub.
b) Ainult II.
c) II ja III.
d) I ja II.
e) II ja IV.
Õige alternatiiv: b) Ainult II.
a) VALE. Vesi on anorgaaniline ühend ja bensiin orgaaniline ühend. Nendel ainetel puudub võime suhelda ja kuna neil on erinev tihedus, moodustavad nad heterogeense segu.
b) ÕIGE. Sool, naatriumkloriid, lahustub vees, moodustades lahuse, mis on homogeenne segu.
c) VALE. Liiv, ränidioksiid, moodustab veega heterogeense segu.
d) VALE. Sool on anorgaaniline ühend ja bensiin orgaaniline ühend. Nendel ainetel puudub võime suhelda ja kuna neil on erinev tihedus, moodustavad nad heterogeense segu.
e) VALE. Liiv on anorgaaniline ühend ja bensiin orgaaniline ühend. Nendel ainetel puudub koostoime võime ja nad moodustavad seetõttu heterogeense segu.
4. (Ufes) Hästi segatud süsteemis, mis koosneb liivast, soolast, suhkrust, veest ja bensiinist, on faaside arv järgmine:
a) 2.
b) 3.
c) 4.
d) 5.
e) 6.
Õige alternatiiv: b) 3.
1. faas: sool ja suhkur suudavad veega suhelda ning molekulidevaheliste jõudude kaudu seonduvad molekulid ja moodustavad lahuse, mis on homogeenne segu.
2. faas: vesi on anorgaaniline ühend ja bensiin orgaaniline ühend. Nendel ainetel puudub võime suhelda ja kuna neil on erinev tihedus, moodustavad nad heterogeense segu.
3. ETAPP: Liiv on silikaat, millel puudub keemiline afiinsus vee ja bensiiniga ning mis seetõttu kujutab endast faasi.
5. (Mackenzie) Segu, mille moodustasid:
a) jääkuubikud ja suhkru vesilahus (glükoos).
b) N gaasi2 ja CO2.
c) vesi ja atsetoon.
d) vesi ja karusmarjasiirup.
e) petrooleum ja diisliõli.
Õige alternatiiv: a) jääkuubikud ja suhkru vesilahus (glükoos).
a) ÕIGE. On võimalik jälgida kahte faasi: jääkuubikud ja glükoosilahus, seega on need heterogeensed süsteemid.
b) VALE. Gaasid on alati homogeenne segu.
c) VALE. Propanooni karbonüüli ja veemolekuli vahel tekivad vesiniksidemed. Kuna need on polaarsed ained, on atsetoon võimeline vees lahustuma ja moodustama homogeense segu.
d) VALE. Need kaks komponenti segunevad, moodustades homogeense süsteemi, kuna karusmarjasiirupist näeme ainult punast vedelikku, kuna lahjendamine toimub vee lisamisega.
e) VALE. Mõlemad on orgaanilised ühendid ja keemilise afiinsuse tõttu moodustavad nad ühe faasi, mis esindavad homogeenset süsteemi.
Kontrollige oma teadmisi harjutustega:
- Harjutused homogeensete ja heterogeensete segude kohta
- Harjutused segude eraldamiseks
- Harjutused aine omaduste kohta

