THE Perioodilisustabel on mudel, mis rühmitab kõik teadaolevad keemilised elemendid ja nende omadused. Need on paigutatud aatomnumbrite (prootonite arv) kasvavas järjekorras.
Kokku on uuel perioodilisustabelil 118 keemilist elementi (92 looduslikku ja 26 kunstlikku).
Iga ruut määrab keemilise elemendi nime, selle sümboli ja aatomi numbri.
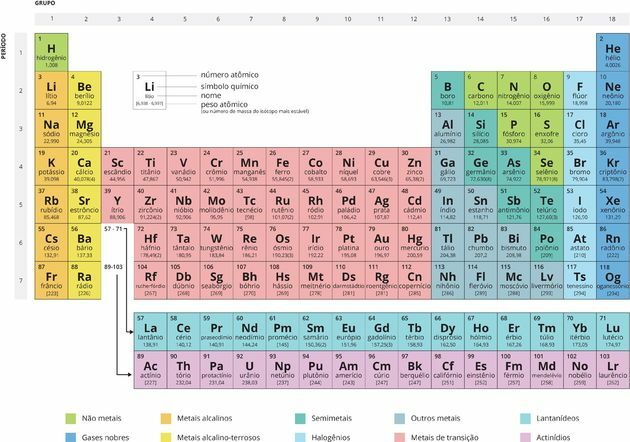
Perioodiliste tabelite korraldamine
kõned Perioodid need on nummerdatud horisontaaljooned, millel on elemendid, millel on sama arv elektroonilisi kihte, kokku seitse perioodi.
- 1. periood: 2 elementi
- 2. periood: 8 elementi
- 3. periood: 8 elementi
- 4. periood: 18 elementi
- 5. periood: 18 elementi
- 6. periood: 32 elementi
- 7. periood: 32 elementi
Tabelis olevate perioodide korralduse korral muutuksid mõned horisontaaljooned väga pikaks, mistõttu on tavaline, et lantaniidide ja aktiiniidide seeriad esindatakse teistest eraldi.
Kell Perekonnad või rühmadesse on vertikaalsed veerud, kus elementidel on sama arv elektrone välimises kestas, see tähendab valentsikiht. Nende rühmade paljud elemendid on omavahel seotud keemilised omadused.
Rühmi (A ja B) on kaheksateist ning tuntumad perekonnad on A-rühmast, mida nimetatakse ka esinduslikud elemendid:
- 1A Perekond: Leeliselised metallid (liitium, naatrium, kaalium, rubiidium, tseesium ja frantium).
- 2A Perekond: Leelismuldmetallid (berüll, magneesium, kaltsium, strontsium, baarium ja raadium).
- 3A Perekond: Booriperekond (boor, alumiinium, gallium, indium, tallium ja nihoonium).
- 4A Perekond: Süsiniku perekond (süsinik, räni, germaanium, tina, plii ja fleroviium).
- 5A Perekond: Lämmastikuperekond (lämmastik, fosfor, arseen, antimon, vismut ja muskovium).
- 6A Perekond: Kalkogeenid (hapnik, väävel, seleen, telluur, poloonium, livermorium).
- 7A Perekond: Halogeenid (fluor, kloor, broom, jood, astatiin ja tenessiin).
- 8A Perekond: Väärisgaasid (Heelium, neoon, argoon, krüpton, ksenoon, radoon ja oganessoonium).
Sina üleminekuelemendid, mida nimetatakse ka siirdemetallideks, esindavad B rühma 8 perekonda:
- 1B perekond: vask, hõbe, kuld ja roentgen.
- 2B perekond: tsink, kaadmium, elavhõbe ja kopernik.
- 3B perekond: skandium, ütrium ja tõsised lantaniidid (15 elementi) ja aktiniidid (15 elementi).
- 4B perekond: titaan, tsirkoonium, hafnium ja ruteerfordium.
- 5B perekond: vanaadium, nioobium, tantaal ja dubnium.
- Perekond 6B: kroom, molübdeen, volfram ja mereaal.
- 7B perekond: mangaan, tehneetsium, reenium ja bohrium.
- 8B perekond: raud, ruteenium, osmium, hassium, koobalt, roodium, iriidium, meitnerium, nikkel, pallaadium, plaatina, darmstaadium.
Rahvusvahelise puhta ja rakendusliku keemia liidu (IUPAC) otsusel hakati gruppe korraldama arvude järgi 1 kuni 18, kuigi endiselt on tavaline leida perekondi, mida kirjeldatakse tähtede ja numbritega, nagu eespool näidatud.
Oluline erinevus, mille IUPACi esitatud uus süsteem tekitas, on see, et perekond 8B vastab perioodilisustabeli rühmadele 8, 9 ja 10.
Must-valge perioodiline tabel
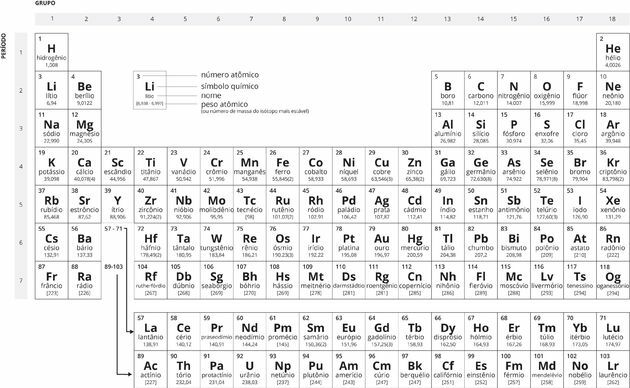
Perioodilise tabeli ajalugu
Tabeli loomise põhieesmärk oli hõlbustada elementide klassifitseerimist, korrastamist ja rühmitamist vastavalt nende omadustele.
Kuni praeguse mudelini jõudmiseni lõid paljud teadlased tabeleid, mis näitasid viisi keemiliste elementide korrastamiseks.
Kõige täieliku perioodilisustabeli koostas vene keemik Dmitri Mendelejev (1834-1907), aastal 1869 tänu aatommass elementidest.
Mendelejev korraldas elementide rühmad sarnaste omaduste järgi ja jättis tühjad ruumid elementidele, mis tema arvates veel avastati.
Perioodilist tabelit, nagu me seda täna teame, korraldas Henry Moseley, 1913. aastal, korraldusega aatomnumber keemilised elemendid, korraldades Mendelejevi pakutud tabeli ümber.
William Ramsay avastasid elemendid neoon, argoon, krüptoon ja ksenoon. Need elemendid koos heeliumi ja radooniga hõlmasid perioodiliste tabelite väärisgaaside perekonda.
Glenn Seaborg avastas transuraansed elemendid (numbrid 94–102) ja tegid 1944. aastal ettepaneku perioodilise tabeli ümberkonfigureerimiseks, asetades aktiniidide seeria lantaniidide sarja alla.
Aastal 2019 saab perioodiline tabel 150 aastat vanaks ning selle aasta tegemiseks loodi ÜRO ja UNESCO resolutsioon Rahvusvaheline keemiliste elementide perioodiline tabel kui viis ühe kõige mõjukama ja olulisema loomingu äratundmiseks teaduse.
Perioodilise tabeli kurioosumid
- Rahvusvaheline puhta ja rakenduskeemia liit Rahvusvaheline puhta ja rakenduskeemia liit - IUPAC) on valitsusväline organisatsioon (valitsusväline organisatsioon), mis tegeleb õpingutega ja edasijõudmisega aastal Keemia. Üle kogu maailma soovitab organisatsioon perioodilisustabeli jaoks kehtestatud standardit.
- 350 aastat tagasi oli laboris esimene isoleeritud keemiline element fosfor Saksa alkeemik Henning Brand.
- Plutooniumi elemendi avastas 1940. aastatel Ameerika keemik Glenn Seaborg. Ta avastas kõik transuraansed elemendid ja võitis 1951. aastal Nobeli preemia. Element 106 sai tema auks nimeks Seaborgium.
- 2016. aastal muudeti laua uued keemilised elemendid ametlikuks: Tennessine (Ununséptio), Nihonium (Ununtrio), Moscovium (Ununpêntio) ja Oganesson (Ununóctio).
- Sünteesitud uusi keemilisi elemente nimetatakse üliraskeks, kuna need sisaldavad palju prootonid, mis on palju parem looduses leiduvatest keemilistest elementidest.
Perioodilise tabeli kokkuvõte
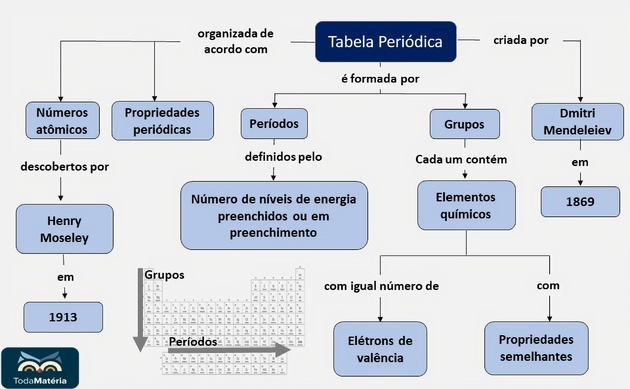
Vaadake sisseastumiseksami küsimusi kommenteeritud resolutsiooniga aastal Harjutused perioodilisustabelis ja avaldamata küsimused Harjutused perioodilise tabeli korraldamiseks.