Adsorptsioon on vedelate, gaasiliste ja tahkete ainete molekulide füüsikalis-keemiline omadus.
Protsess toimub siis, kui vedelad või gaasilised osakesed jäävad tahkete ainete pinnale kinni. Kui tahked ained on poorsed, suureneb adsorptsioonivõime veelgi.
Protsessis osalevate komponentide jaoks on kaks klassifikatsiooni:
- Adsorbandid: See on vedel või gaasiline aine, mis jääb adsorbeeriva tahke aine pinnale.
- Adsorbendid: See on tahke aine, mis soodustab teiste ainete kinnipidamist.
THE desorptsioon see on adsorptsiooni pöördprotsess, see tähendab adsorbaadi eraldumist adsorbendi pinnalt.
Tüübid
Sõltuvalt protsessis osalevate jõudude olemusest võib adsorptsioon olla kahte tüüpi: füüsisorptsioon ja kemisorptsioon.
Mõnel juhul võib mõlemat tüüpi adsorptsioon toimuda samas protsessis.
füüsikaline imendumine
Füüsiline füüsikaline adsorptsioon või adsorptsioon adsorbaadi ja adsorbendi vahel toimub Van der Waallsi jõudude (dipool-dipool või indutseeritud dipool) kaudu.
Sellisel juhul ei esine protsessis osalevate ainete molekulaarset muutust. See tähendab, et aine säilitab oma keemilise olemuse.
Füüsiline adsorptsioon on pöörduv protsess.
Kemisorptsioon
Kememisorptsioon ehk keemiline adsorptsioon koosneb a keemiline reaktsioon. Kaasates elektronid, peetakse tugevamaks keemiliseks sidemeks kui füüsisorptsioon.
Kememisorptsioonis toimub protsessis osalevate ainete molekulaarne muutus. See tähendab, et ainet saab teisendada.
Kuna tegemist on keemilise reaktsiooniga, peavad adsorbendi ja adsorbaadi komponendid olema spetsiifilised. Nad peavad suutma ära tunda ja reageerida.
Keemiline adsorptsioon on pöördumatu protsess.
Loe ka:
- Molekulidevahelised jõud
- Keemilised sidemed
Adsorptsioon ja imendumine
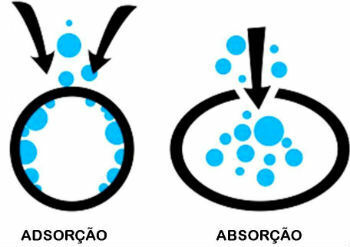
Erinevus adsorptsiooni ja neeldumise vahel
Adsorptsioon ja imendumine on kaks erinevat protsessi. Teadke nende erinevust:
- adsorptsioon: Aine jääb teise pinnale, ilma et see oleks osa selle mahust.
- Imendumine: Üht ainet imab teine, põhjustades mahu muutust.
Levinud imendumise näide on vett imav käsn. Seda tehes lisatakse vee maht käsna mahtu.
Aktiveeritud süsi
Aktiivsüsi on näide tuntumatest adsorbentidest. Selle struktuuris on arvukalt poore, mis intensiivistavad ainete kinnipidamist ja suurendavad nende adsorptsioonivõimet.
Seetõttu kasutatakse aktiivsütt orgaaniliste ainete, õlide, värvainete ja lõhnade eemaldamiseks. Seda kasutatakse ka veepuhastuseks ning kosmeetika ja ravimite valmistamiseks.

Aktiveeritud süsi
Loe ka:
- Kromatograafia
- Segude eraldamine
- Soluut ja lahusti
- Keemia laboris kasutatud materjalid