Kell orgaanilised eliminatsioonireaktsioonid on need, milles molekuli aatomid või aatomirühmad eemaldatakse või elimineeritakse sellest, uue orgaanilise ühendi loomine, lisaks anorgaanilisele ühendile, mis moodustub osast, mis oli kustutatud.
Üks eliminatsioonireaktsiooni tüüp on dehüdratsioon, milles kadunud molekul on vesi. Alkoholide (ühendid, millel on avatud ahelas küllastunud süsinikuga seotud OH-rühm) dehüdratsioon võib toimuda kahel viisil: molekulisisese ja molekulidevahelise.
"Intra" tähendab "sees", seetõttu alkoholide molekulisisese dehüdratsioon toimub siis, kui veemolekul väljub alkoholi molekuli enda seest. Sel juhul on moodustunud orgaaniliseks tooteks alkeen.
See reaktsioon toimub ainult kuivatusainena toimiva katalüsaatori juuresolekul ja enamasti on see kontsentreeritud väävelhape (H2AINULT4) ja temperatuur peaks olema umbes 170 ºC.
Näide:
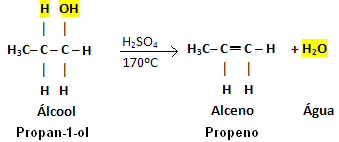
Pange tähele, et OH-rühm lahkus ja vesinik lahkus naabersüsinikust, põhjustades vett. Lisaks loodi kaksikside, millest tekkis alkeen.
Dehüdratsiooni all kannatav rajatis järgmiselt kahanevas järjekorras:
Tertsiaarsed alkoholid> Sekundaarsed alkoholid> Primaarsed alkoholid
Aga mis saab siis, kui OH-rühm tuleb süsinikuahela keskele? Vesinikuaatom, millest naabersüsinikuaatom vabaneb ja moodustab veemolekuli?
Ärge lõpetage kohe... Peale reklaami on veel;)
Näiteks on järgmine 2-metüülpentaan-3-ool. Pange tähele, et üks naabruses asuv süsinikuaatom on tertsiaarne (esile tõstetud punasega), teine aga sekundaarne (esile tõstetud sinisega):
H OH H
│ │ │
H3C─ Ç ─ Ç ─ Ç CH3
│ │ │
H H CH3
Tertsiaarse süsinikuaatomiga seotud vesinikku on kergem jätta, kuna selle elektronegatiivne iseloom on võrdne δ+1Seega, mida vähem negatiivne on süsiniku iseloom, seda nõrgem on nende omavaheline side ja seda lihtsam on nende side katkestada.
Sellistel juhtudel moodustuvad kõik võimalikud ühendid, kuid ülekaal antakse järgmises järjekorras: Tertsiaarsed alkoholid> Sekundaarsed alkoholid> Primaarsed alkoholid.
Nii et meil on:
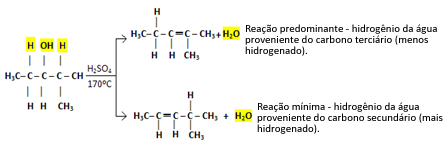
Seda tüüpi reaktsioonid alluvad Saytzefi reegel, mis seda ütleb on suurem tendents, et vesinik jätab süsiniku vähem hüdrogeenitud. See reegel on täpselt vastupidine Markovnikovi reegel kasutatakse liitumisreaktsioonide jaoks.
Oma teadmiste täiendamiseks sellel teemal lugege ka teksti "Alkoholide molekulidevaheline dehüdratsioon”.
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Alkoholide molekulidevaheline dehüdratsioon"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm. Juurdepääs 28. juunil 2021.