Kell kovalentsed sidemed, nimetatud ka molekulaarsed või homopolaarsed sidemedon need, mis esinevad aatomite vahel elektronegatiivsed elemendid, see tähendab kalduvusega elektrone vastu võtta, luues seose jagades oma valentskestadest elektrone.
Kovalentne side võib tekkida järgmiste elementide vahel: vesinik, mittemetallid ja poolmetallid. Metallid ei osale kunagi seda tüüpi sidumises.
Vaatleme kovalentse sideme lihtsat näidet: gaasi moodustavat vesiniksidet (H2):
H + H → H2
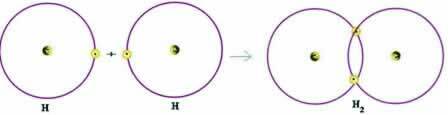
Pange tähele, et mõlemad aatomid vajasid elektrooni saamiseks valentskesta lõpuleviimist - vastavalt oktettide reeglile - ja sel viisil püsimiseks. Seetõttu jagasid nad oma elektrone ja nii oli mõlemal kaks elektroni, neil oli täielik K-kest ja omandati väärisgaasheeliumi konfiguratsioon.
See elektronide jagamine eristab seda tüüpi sidemeid ioonsidestustest, milles toimub elektronide ülekanne.
Selle juhtumi veel kaks näidet leiate allolevalt jooniselt:
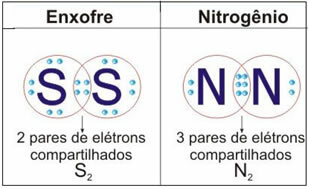
Ärge lõpetage kohe... Peale reklaami on veel;)
Seda tüüpi sidemetes moodustuvad molekulid, mida saab esindada nende vastavate sidemetega
molekulaarsed valemid, see tähendab kõige lihtsam kujutis, mis näitab, kui palju on iga elemendi aatomeid molekulis. Mõned molekulivalemite näited on: H2, S2, O2, ei2, H2O, CO2, jne.Kovalentset sidet saab esitada kahe teise valemiga:
- Elektrooniline valem või Lewise valem: selles valemis ilmuvad ka iga aatomi valentskesta elektronid ja moodustuvad elektroonilised paarid. Neid elektrone sümboliseerivad märgid . või x;
- Tasane struktuurivalem või siduri struktuurivalem: näitab elementide linke, kusjuures iga jagatud paar vastab kriipsule. Kui see on lihtsalt kriips, nimetame seda üheks lingiks; kui neid on kaks, siis kaksikside; ja kui on kolm kriipsu, siis kolmekordne side.
Pange tähele muid näiteid kovalentsete sidemete esitamisest nende kolme keemilise valemiga:
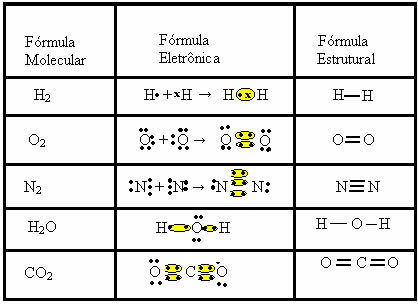
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Kovalentsed sidemed"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. Juurdepääs 27. juunil 2021.