O arvutamine aatommass Elemendi väärtus on matemaatiline ressurss, mida kasutatakse iga olemasoleva keemilise elemendi perioodilisustabelis sisalduva massi väärtuse määramiseks. Üldiselt teostada aatommassi arvutamine, peame teadma järgmisi muutujaid keemiline element:
Elementide isotoopid;
Elemendi iga isotoobi massinumber;
Elemendi iga isotoobi protsent looduses.
Näiteks vesiniku aatommass arvutati järgmiste andmete põhjal:
Esitab protiumi isotoope (H1), deuteerium (H2) ja triitiumi (H3);
Nende isotoopide massid on vastavalt 1, 2 ja 3;
Protiumi protsent looduses on 98,9%;
Deuteeriumi protsent looduses on 0,09%;
Tritiumprotsent looduses on 0,01%.
Matemaatiline standard aatommassi arvutamiseks
Et teostada aatommassi arvutamine mis tahes keemilise elemendi puhul peame kasutama järgmist matemaatilist mustrit:
1O: korrutatakse iga isotoobi massinumber protsendiga;
2O: lisage kõik esimese astme korrutustega leitud tulemused;
3O: jagage leitud summa 100-ga.
M.A. massinumber.protsent + massinumber.protsent
100
Meelekaart: aatomimissa
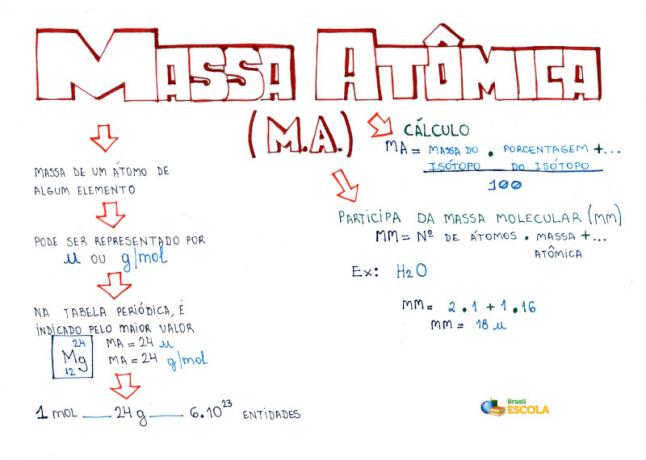
* Mõttekaardi allalaadimiseks PDF-failina Kliki siia!
Aatomimassi arvutamise näited
⇒ 1. näide: Väävli aatommassi arvutamine.
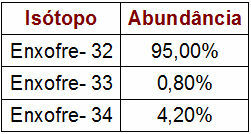
Väävelisotoopide protsent ja massiandmed
Esitatud tabel näitab iga looduses sisalduva väävli isotoobi massi arvu ja protsenti. Aatommassi arvutamiseks toimige lihtsalt järgmiselt.
1O Samm: korrutage iga isotoobi massiarv selle arvukuse väärtusega.
Väävel - 32 (S32)
s32 = 32.95
s32 = 3040
Väävel - 33 (S33)
s33 = 33.0,8
s33 = 26,4
Väävel - 34 (S34)
s34 = 34.4,2
s34 = 142,8
2O Samm: liidetakse väärtused, mis on leitud massinumbri ja isotoobi arvukuse korrutistes.
Summa = S32 + S33 + S34
Summa = 3040 + 26,4 + 142,8
Summa = 3209,2
3O Samm: arvutage aatommass jagades leitud tulemuste summa 100-ga:
M.A. Summa
100
M.A. 3209,2
100
M.A. = 32,092 u
⇒ 2. näide: Antud keemilisel elemendil (D) on kolm isotoopi, mille massinumbrid on:
30D 32D 34D
Teades, et selle elemendi aatommass on 32,20 u ja isotoopi on 20% 32D on looduses D, mis on teiste isotoopide protsentide väärtus?
Lauses on toodud ühe isotoopi massinumbrid, aatommass ja protsent. Teiste isotoopide protsentide määramiseks peame tegema järgmised sammud:
1O Samm: määrata iga isotoobi protsent.
Isotoop - 30 (DS30)
DS30 = 30.x
DS30 = 30x
Isotoop - 32 (DS32)
DS32 = 32.20
DS32 = 640
Isotoop - 34 (D34)
DS34 = 34.y
DS34 = 34a
2O Samm: aatomimassi arvutamiseks kasutage kõiki matemaatilises avaldises leiduvaid andmeid.
M.A. massinumber.protsent + massinumber.protsent
100
32,2 = 30x + 640 + 34a
100
32,2.100 = 30x + 640 + 34a
100
3220 - 640 = 30x + 34a
30x + 34y = 2580
x = 2580 - 34a
30
3O Samm: kasutage ülaltoodud väljendit järgmiselt:
Isotoobi 1 protsent + isotoobi 2 protsent + isotoobi 3 protsent = 100%
x + 20 + y = 100
x + y = 100-20
x + y = 80
x = 80 - y
2580 - 34a = 80-aastane
30
2580 - 34y = 30. (80-a)
2580–34 a = 2400–30 aastat
2580–2400 = 34–30 aastat
4y = 180
y = 80
4
y = 45%
4O Samm: arvutage kolmandas etapis koostatud avaldises protsent x väärtusest.
x + y = 80
x + 45 = 80
x = 80–45
x = 35%
Minu poolt. Diogo Lopes Dias
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm
