Cuando el anillo de benceno ya tiene un sustituyente, este radical influirá en todas las demás sustituciones de H en el anillo. Este sustituto puede ser orto y para-director o meta-director. Pero surgen las preguntas:
| ¿Qué hace que el grupo unido al anillo de benceno influya en la dirección y reactividad de la reacción de sustitución? |
| ¿Qué hace que ciertos grupos sean consejeros de objetivos (incapacitantes) y otros orto-para (activadores)? |
Estas dos preguntas se responden entendiendo los llamamientos. efectos electronicos que estos grupos ejercen en el ring. Este efecto se produce debido a la diferencia de electronegatividad entre los elementos, ya que el sustituyente polarizan los enlaces del núcleo aromático, induciendo alternativamente un carácter positivo en algunos carbonos del anillo, mientras que otros permanecen con un carácter negativo.
| Se producirá una nueva sustitución en los átomos de carbono que tienen carácter negativo. |
Veamos cómo se producen estos efectos electrónicos en el anillo aromático, teniendo en cuenta el orden de electronegatividad de los elementos: F> O> N> Cl> Br> S> C> I> H.
1er caso: Radical activador u orto-director:
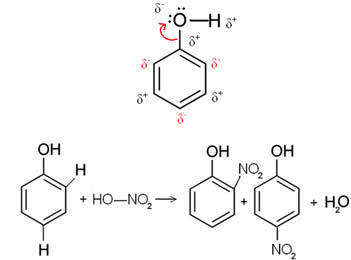
Por ejemplo, en el caso debajo de la molécula de benzol (fenol), el oxígeno es el elemento más electronegativo, por lo que atrae electrones hacia sí mismo, lo que hace que el carbono tenga una carga parcialmente positiva, lo que induce polarización de anillo alternante. Las posiciones negativas son exactamente las posiciones orto y para. Por eso el grupo -OH es un radical activador u orto-a-directores. Esto se puede ver en la reacción de nitración de fenol a continuación, dando lugar a o-nitrofenol y p-nitrofenol como productos:
No pares ahora... Hay más después de la publicidad;)
2do caso: desactivando radical o meta-líder:
Ahora considere el caso del nitrobenceno:
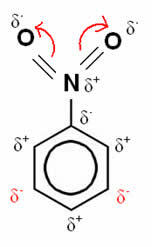
En este ejemplo, el oxígeno sigue siendo el elemento más electronegativo, por lo que atrae los enlaces formados con el nitrógeno hacia sí mismo, que está parcialmente cargado positivamente, lo que induce al átomo de carbono unido a que se polarice negativamente y, por lo tanto, sucesivamente. Así, la posición que se vuelve negativa y más susceptible de sustitución es la posición objetivo, siendo, por tanto, un inhabilitando.
Vea ahora con más detalle este efecto electrónico, que se llama efecto resonante.
| efecto resonante es la atracción o repulsión de electrones en enlaces π (pi) de enlaces dobles o triples, cuando resuenan con el propio anillo de benceno. |
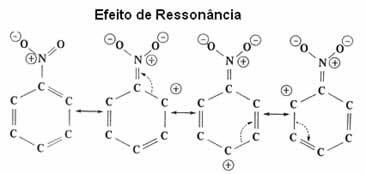
Como se ve, el grupo NO2 está desactivando el anillo, ya que está tomando electrones de él y disminuyendo su densidad de electrones. Por lo tanto, el grupo que atacará y hará la sustitución (electrófilo) es positivo, por lo que atacará preferentemente la meta posición que obtuvo una carga negativa.
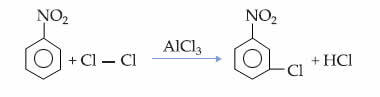
Este hecho se puede ver en la reacción de monocloración del nitrobenceno, en la que la sustitución ocurre solo en la posición meta:
Por Jennifer Fogaça
Licenciada en Química
Equipo Escolar de Brasil
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Efectos electrónicos de radicales meta y orto-directores"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm. Consultado el 28 de junio de 2021.



