O Diagrama de fases es un gráfico que se utiliza para indicar las condiciones de temperatura y presión necesitaba conseguir un sustancia en cierto estado fisico (sólido, líquido o gaseoso).
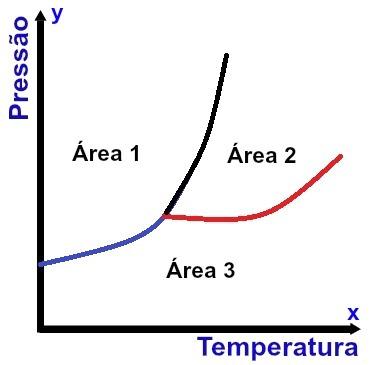
Representación de un diagrama de fases
El eje x (horizontal) contiene valores de temperatura y el eje y (vertical) contiene valores de presión. Además, hay tres curvas conectadas a un solo punto (llamado punto triple), dividiendo el gráfico en tres áreas bien definidas, como se puede ver en el diagrama que se muestra arriba.
Además de indicar las condiciones para que la sustancia se encuentre en un estado físico específico, el Diagrama de fases indica las condiciones para que se produzca cualquier cambio en el estado físico.
Los cambios de estado físico son:
Fusión: transición de estado sólido a líquido;
Solidificación: transición de estado líquido a sólido;
Vaporización: transición de estado líquido a gaseoso;
Condensación: transición de estado gaseoso a líquido;
Sublimación: transición de estado sólido a gaseoso;
Resublimación: transición de gas a estado sólido.
a) Regiones
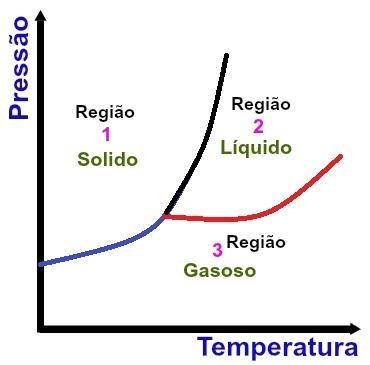
Regiones fundamentales de un diagrama de fases
Región 1
La región 1 indica las condiciones de temperatura y presión en las que encontramos la sustancia en estado sólido.
Región 2
La región 2 indica las condiciones de temperatura y presión en las que encontramos la sustancia en estado líquido.
Región 3
La región 3 indica las condiciones de temperatura y presión en las que encontramos la sustancia en estado gaseoso.
b) Curvas

Curvas presentes en un diagrama de fases.
Curva A (curva morada)
Es la curva que divide la región sólida y gaseosa del diagrama de fase y comúnmente se llama curva de resublimación. Cada punto ubicado en la curva 1 indica que tenemos una determinada sustancia coexistiendo en estado sólido y gaseoso.
No pares ahora... Hay más después de la publicidad;)
Además de indicar coexistencia, la curva 2 también indica las condiciones de temperatura y presión para la transformación de una sustancia de estado líquido a gaseoso.
Curva B (curva negra)
Es la curva que divide la región sólida y líquida del diagrama de fases y se denomina comúnmente curva de solidificación. Cada punto ubicado en la curva 2 indica que tenemos una determinada sustancia coexistiendo en estado sólido y gaseoso.
Además de indicar coexistencia, la curva 2 también indica las condiciones de temperatura y presión para la transformación de una sustancia que se encuentra en estado líquido a estado sólido.
Curva C (curva roja)
Es la curva que divide la región sólida y gaseosa del diagrama de fase y comúnmente se llama curva de condensación. Cada punto ubicado en la curva 3 indica que tenemos una determinada sustancia coexistiendo en estado sólido y gaseoso.
Además de indicar coexistencia, la curva 3 también indica las condiciones de temperatura y presión para la transformación de una sustancia de estado sólido a gaseoso y viceversa.
c) El punto triple
El punto donde se encuentran las tres curvas en el diagrama de fase se llama punto triple. En este punto, tenemos el valor de temperatura y el valor de presión en el que encontramos la sustancia en estado sólido, líquido y gaseoso al mismo tiempo.

d) Cambios de estado físico en el diagrama de fases
En el siguiente diagrama de fases, tenemos 6 flechas que indican la dirección de los cambios en los estados físicos de una sustancia.

Flecha 1: indica la fusión
Flecha 2: indica solidificación
Flecha 3: indica vaporización
Flecha 4: indica condensación
Flecha 5: indica sublimación
Flecha 6: indica resublimación
Por mí. Diogo Lopes Dias
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
DÍAS, Diogo Lopes. "¿Qué es un diagrama de fases?"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-diagrama-fases.htm. Consultado el 28 de junio de 2021.
Química

Transformaciones líquidas, evaporación, fuerzas intermoleculares, supercongelación líquida, cristalización líquida, enfriamiento repentino, viscosidad del líquido, presión de vapor del líquido, presión atmosférica, congelación del líquido, temperatura
Química

Líquidos, tensión superficial, fusión de un sólido, condensación de un gas, viscosidad, fluido, volumen constante, moléculas de un gas, fuerzas intermoleculares, compresión, evaporación de un líquido.

