A amidas son compuestos orgánicos caracterizados por presencia de un nitrógeno (N) unido directamente a un carbonilo (C = O). Se trata de sustancias disponibles de forma natural, una de ellas se encuentra en las excretas de los mamíferos (urea), pero también pueden obtenerse por síntesis artificial.
Las amidas se pueden producir, por ejemplo, por deshidratación de sal de amonio, proceso utilizado en la fabricación de polímeros. También se utilizan como fertilizantes, debido a su disponibilidad de nitrógenos, y cómo fármaco, que tiene acción antimicrobiana.
Lea mas:Acrilamida: amida que se puede originar al calentar algunos alimentos.
Estructura amida
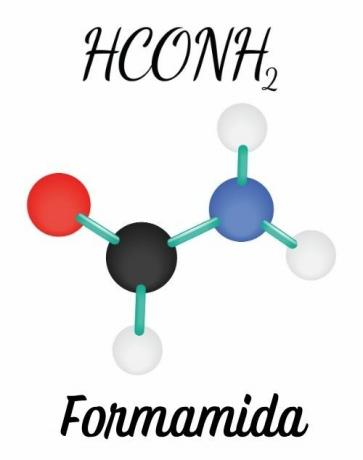
Las amidas están formadas por un nitrógeno unido directamente a un grupo carbonilo o acilo (R-C = O). El doble enlace entre el carbón es el oxígeno y la posibilidad de mover este par al nitrógeno dan a la molécula geometría plana, a diferencia de las aminas, que tienen geometría piramidal.
Clasificación de amidas
Clasificación según el número de sustituyentes orgánicos
Así como el aminas, las amidas se clasifican según el número de radicales orgánicos de sustitución que tiene el nitrógeno, sin embargo, para las amidas, tenemos que considerar que uno de los ligandos del grupo será el grupo acilo, es decir, solo tendremos amidas del tipo:
- Amida no sustituida: tiene nitrógeno unido a dos hidrógenos y un grupo carbonilo.
Ejemplo:

- Amina monosustituida: tiene nitrógeno unido a un hidrógeno, un grupo carbonilo y un radical orgánico. En este caso, donde uno de los hidrógenos ha sido reemplazado por una cadena de carbono, considere R como un grupo orgánico.
Ejemplo:

- Amina disustituida: tiene nitrógeno unido a dos radicales orgánicos y un carbonilo. En este caso, los dos hidrógenos fueron reemplazados por cadenas de carbono.
Ejemplo:

Vea también: ¿Cómo clasificar los haluros orgánicos?
Clasificación según el número de carbonilos ligados al nitrógeno
Las amidas también se pueden clasificar según el número de carbonilos unidos directamente al nitrógeno de la molécula.
- Amidas primarias: solo un grupo acilo unido al nitrógeno (R-CO) NH2 .
- amidas secundarias: dos carbonilos o grupos acilo unidos a nitrógeno (R-CO)2NUEVA HAMPSHIRE.
- amidas terciarias: tres grupos acilo unidos al nitrógeno (R-CO)3No.

Nomenclatura de amidas
LA nomenclatura para amidas será dado por:
prefijo que indica el número de carbonos en la cadena + ubicación e infijo que indica insaturaciones (si las hay) + terminación de amida |
Vea la tabla a continuación:
Prefijo (no. De carbonos) |
Infijo (saturación de cadena) |
Sufijo (grupo funcional) |
|||
1 carbono |
Reunió- |
Solo llamadas individuales |
-un- |
amidas |
-amida |
2 carbonos |
Et- |
||||
3 carbonos |
Apuntalar- |
1 doble enlace |
-en- |
||
4 carbonos |
Pero- |
||||
5 carbonos |
encerrado- |
2 dobles enlaces |
-dien- |
||
6 carbonos |
Maleficio- |
||||
7 carbonos |
Hept- |
1 triple enlace |
-en- |
||
8 carbonos |
Oct- |
||||
9 carbonos |
No- |
2 triples enlaces |
-diin- |
||
10 carbonos |
Dic- |
El recuento de carbono debe comenzar con el lado más cercano al nitrógeno del grupo funcional.
Ejemplos de:
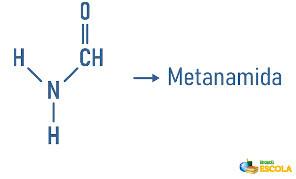



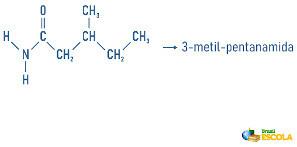
Las aminas también pueden recibir en su nomenclatura una especificación sobre la clasificación de la molécula:
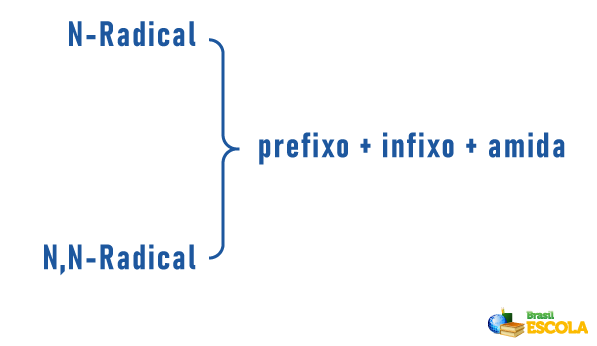
Recordando que la nomenclatura de los radicales está formada por: PAGrefija que indica el número de carbonos + terminación “il” o “ila”. Los radicales se colocan en la nomenclatura en orden alfabético.
Ejemplos de:


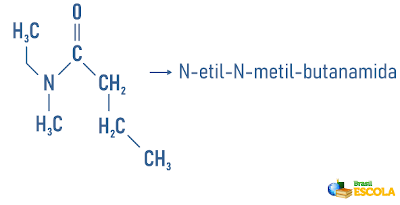
También acceda a: Nomenclatura de hidrocarburos cíclicos y ramificados
Propiedades de las amidas
- Alto punto de fusión y ebullición, que tendrá un valor escalado según el tamaño y la disposición espacial de la cadena de carbono.
- Altamente polar debido a la presencia de carbonilo y nitrógeno.
- Enlace de hidrógeno de amidas no sustituidas y monosustituidas.
- Las moléculas más pequeñas y simples son solubles en agua. El tamaño de la molécula también interfiere con la solubilidad de las amidas: cuanto más grande sea la cadena de carbono, menos solubles serán en agua.
- Las amidas tienen un carácter básico debido a su propensión a recibir iones H+.
Aplicación de amidas
- Utilizados como intermediarios en la fabricación de polietilenos como el nailon.
- Aplicado en la formulación de fármacos como la sulfanilamida y la penicilina, principios activos de fármacos bactericidas para el control de infecciones.
- La urea, que puede obtenerse sintéticamente o como un producto excretado por mamíferos, es una sustancia del grupo amida, una diamida. Se utiliza como complemento alimenticio en agricultura y como fertilizante.

Obteniendo las amidas
Las amidas se encuentran fácilmente en forma natural, pero su forma sintética todavía se usa ampliamente en procesos industriales. A continuación se muestran algunas reacciones de producción de amidas basadas en otros compuestos nitrogenados.
Reacción de deshidratación de sal de amonio

Reacción de aminas con cloruro de ácido.
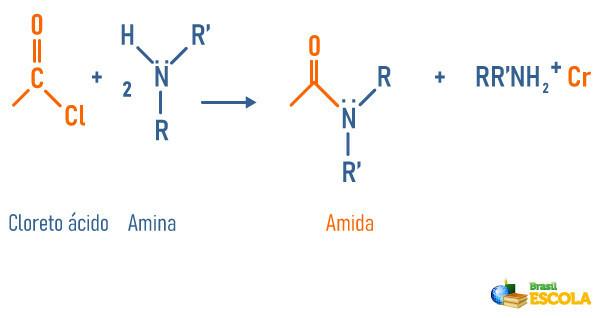
-
Reacción de anhídridos con aminas.
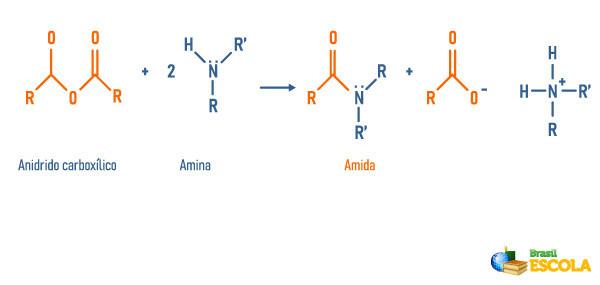
Reacción de ésteres con aminas.

Reordenamiento estructural de una aldoxima
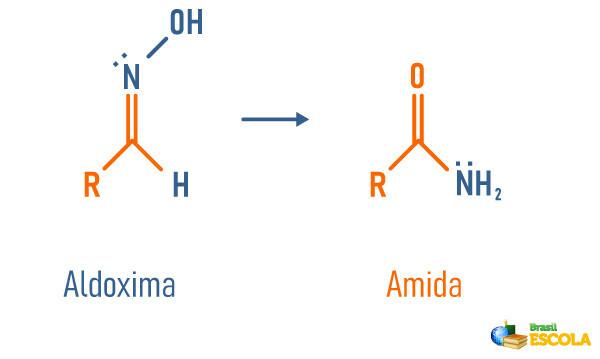
-
Hidratación de nitrilo
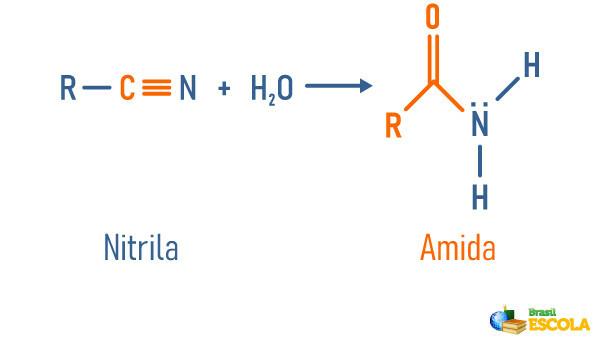
Lea también: Hidrólisis de amida: reacción utilizada para obtener sustancias importantes.
ejercicios resueltos
Pregunta 1 - (UFRS) El aspartamo, que se muestra a continuación, es un edulcorante artificial que se usa en muchos refrescos y alimentos bajos en calorías.

El grupo enmarcado en la figura es característico de la función orgánica
A) éster.
B) amida.
C) aminoácido.
D) amina.
E) carbohidrato.
Resolución
Alternativa B. El grupo funcional seleccionado en la figura es una amida, debido a la presencia de un carbonilo (C = O) unido directamente al nitrógeno (N).
Pregunta 2 - (UNESP) En agosto de 2005 se informó de la incautación de lotes de lidocaína que habrían causado la muerte de varias personas en Brasil, por problemas de fabricación. Este fármaco es un anestésico local ampliamente utilizado en exámenes endoscópicos, lo que reduce la incomodidad del paciente. Su estructura molecular se muestra a continuación:
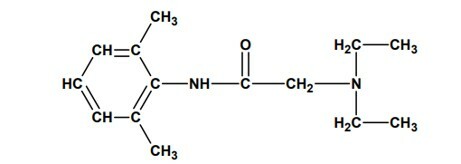
y presenta las funciones:
A) amina secundaria y amina terciaria.
B) amida y amina terciaria.
C) amida y éster.
D) éster y amina terciaria.
E) éster y amina secundaria.
Resolución
Alternativa B.
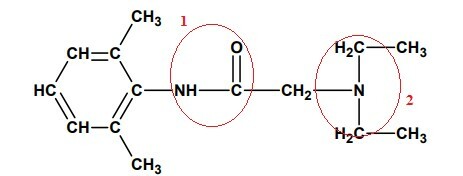
Después de seleccionar y numerar las partes características de cada función orgánica, analicemos cada una:
1- Es un AMIDA debido a la presencia del grupo acilo, (R-C = O) ligado directamente al nitrógeno, monosustituido.
2- Como no tenemos la presencia del grupo acilo (R-C = O), sino solo el nitrógeno unido directamente a otros carbonos de este grupo tenemos una AMINA TERCIARIA, porque los tres hidrógenos, previamente unidos al nitrógeno, han sido reemplazados por grupos Orgánico.
Por Laysa Bernardes Marques de Araújo
Profesor de química

