Tú óxidos anfóteros son óxidos que tienen un comportamiento ambiguo, porque frente a un ácido se comportan como un óxido básico; y en presencia de una base se comportan como óxidos ácidos.
Tanto la base como el ácido con el que reaccionan los óxidos anfóteros deben ser fuertes, con un carácter químico muy pronunciado.
Los óxidos anfóteros son generalmente sólidos iónicos, poco solubles en agua, y cuando reaccionan con estos ácidos y bases fuertes, producen agua y sal.
En general, tenemos:
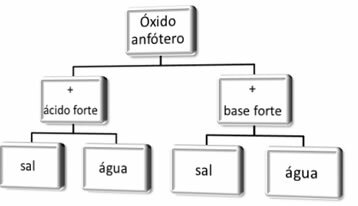
Esquema de reacción de óxidos anfóteros.
Las siguientes son reacciones que involucran dos óxidos anfóteros, óxido de zinc (ZnO) y óxido de aluminio (Al2O3). Nótese cómo en determinadas situaciones reaccionan como ácidos y en otras se presentan como bases:
1er caso: al reaccionar con ácidos fuertes: se comportan como óxidos básicos, produciendo sal y agua
Agua salada ácida de óxido
fuerte anfótero
(base)
ZnO(s) + H2SOLO4 (aq) → ZnSO4 (aq) + H2O(1)
Al2O3 (s) + 6 HCl(aquí) → 2 AlCl3 (aq) + 3 H2O(1)
2do caso: al reaccionar con bases fuertes: se comportan como óxidos ácidos, produciendo sal y agua
Agua salada a base de óxido
fuerte anfótero
(ácido)
ZnO(s) + 2NaOH(aquí) → En2ZnO2 (aq) + H2O(1)
Alabama2O3 (s) + 2 KOH(aquí) → 2 KAlO2 (aq) + H2O(1)
Los principales óxidos anfóteros son el zinc y el aluminio; incluyendo óxido de zinc (ZnO), también conocido como alvaid, es un polvo blanco, amorfo, inodoro, insoluble en agua, pero soluble en soluciones ácidas, que se utiliza para pintar caras de payasos. También se utiliza como astringente y protector solar en forma de loción, pomada y gelatina.

Payaso aplicando cal (óxido de zinc) como maquillaje
También existen óxidos de otros metales (SnO y SnO2, PbO y PbO2) y no metales (como2O3, A2O5, se sentó2O3, se sentó2O3).
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/oxidos-anfoteros.htm


