Para clasificar un enlace sigma, es fundamental saber reconocerlo en la estructura de una molécula. El enlace sigma es en realidad un enlace covalente que ocurre cuando dos orbitales atómicos incompletos (con un solo electrón) interpenetrar en el mismo eje. Un ejemplo es cuando un orbital de tipo p (hélice) interpenetra con otro orbital p.

orbitales p interpenetrados en un enlace sigma p-p
En la práctica (en ejercicios), el reconocimiento y clasificación de un enlace sigma se realiza a partir de la fórmula estructural de una sustancia, como en la siguiente representación estructural:

Fórmula estructural de ácido cianhídrico
Antes de clasificar un enlace sigma, hay que saber reconocerlo en una fórmula estructural. Para esto, solo recuerda el maneras como un enlace covalente es representado: la llamada sencillo está representado por un solo guión (-), el par está representado por dos (=) y el enlace triple está representado por tres (≡). El enlace sigma está presente en cualquiera de las tres representaciones de enlaces covalentes de la siguiente manera:
Sencillo: tiene un enlace sigma;
Par: De los dos enlaces, solo uno es sigma;
Triple: Uno de los tres enlaces es sigma.
Sabiendo cómo reconocer un enlace sigma, el siguiente paso es aprender a clasificarlo. Para ello, debemos saber cuál es el orbital incompleto de cada átomo involucrado en el enlace:
H - presenta el orbital s incompleto, por lo tanto, en la clasificación, está representado por s.
Ametals- tienen un orbital p incompleto, por lo que, en la clasificación, están representados por p, con la excepción de los siguientes elementos:
Carbón: Su orbital incompleto depende del tipo de hibridación que sufre. Las posibilidades son: hibridación sp3 (cuánto cuesta cuatro simples llamadas), sp2 (cuánto forman dos enlaces simples y uno doble) o sp (cuánto lleva a cabo dos dobles enlaces o uno simple y uno triple). Por lo tanto, en la clasificación de un enlace sigma, el carbono se puede representar por sp3, sp2 o sp dependiendo de la llamada que esté realizando.
Berilio:sufrir hibridación de tipo sp, así, en la clasificación, está representado por sp.
Boro:sufrir hibridación de tipo sp2, así, en la clasificación, está representado por sp.2.
Con toda esta información, la parte más sencilla es clasificar los enlaces sigma presentes en una estructura. Veamos algunos ejemplos:
Ejemplo 1: conexiones sigma en el agua

Fórmula estructural del agua
La fórmula estructural anterior muestra que el agua tiene dos enlaces sigma (dos simples), siendo ellos entre el oxigeno (representado por p) es el Hidrógeno (representado por s). Así, tenemos dos enlaces sigma clasificados en:
s-p
Ejemplo 2: Enlaces sigma en tricloruro de fósforo

Fórmula estructural del tricloruro de fósforo.
La fórmula estructural anterior muestra que el tricloruro de fósforo tiene tres llamadassigmas (tres simples), siendo ellos entrar en el fósforo (representado por p) es el cloro (representado por p). Así, tenemos tres enlaces sigma clasificados en:
páginas
Ejemplo 3: enlaces sigma en trifluoruro de boro
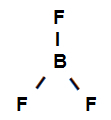
Fórmula estructural de trifluoruro de boro
La fórmula estructural anterior muestra que el trifluoruro de boro tiene tres enlaces sigma (tres simples), siendo ellos entrar en el boro (representado por sp2) es el Flúor (representado por p). Así, tenemos tres enlaces sigma clasificados en:
p-sp2
Ejemplo 4: enlaces sigma en etanol
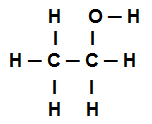
Fórmula estructural de etanol
La fórmula estructural para el etanol anterior muestra que contamos con la presencia de ocho convocatorias sigmas (ocho enlaces simples). Son ellas:
Uno entre el Oxigeno (representado por p) y el hidrogeno (representado por s). Por lo tanto, el enlace se clasifica en sigma s-p.
Uno de dos carbonos que realizan solo conexiones sigma (y luego representado por sp3). Por tanto, el enlace se clasifica en sp3-PAG3.
Uno entre el Carbono (representado por sp3) y el oxigeno (representado por p). Por lo tanto, el enlace sigma se clasifica en p-sp3.
cinco entre carbono (representado por sp3) y el hidrogeno (representado por s). Por lo tanto, los cinco se clasifican en s-sp3.
Ejemplo 5: Enlaces sigma en dicloroeteno

Fórmula estructural de dicloroeteno
La fórmula estructural del dicloroeteno anterior muestra que tenemos la presencia de cinco enlaces sigma (los cuatro enlaces simples y uno de los enlaces dobles). Son ellas:
Uno de dos carbonos que realizan dos enlaces simples y uno doble (y luego representado por sp2). Por lo tanto, el enlace sigma se clasifica en sp2-PAG2.
Cuatro están entre carbono(representado por sp2)y el hidrogeno (representado por s). Así, los cuatro se clasifican en s-sp2.
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/classificacao-uma-ligacao-sigma.htm