O punto de fusión y ebullición son, respectivamente, las temperaturas a las que los materiales cambian de sólido a líquido y de líquido. para el gas o la temperatura máxima a la que el líquido puede permanecer en este estado físico en un determinado presión.
Los puntos de fusión y ebullición de los elementos químicos de la tabla periódica varían según sus números atómicos, lo que significa que son propiedades periódicas.
En la tabla periódica, el orden de crecimiento de las temperaturas de fusión y ebullición de los elementos químicos sigue el siguiente esquema de flechas:
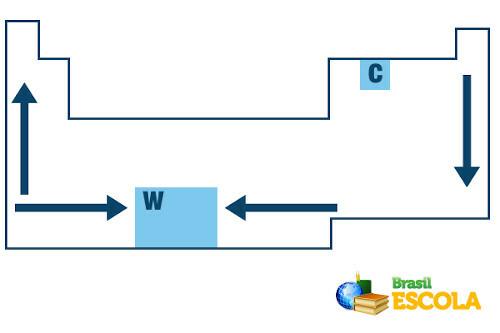
Crecimiento del punto de fusión y de ebullición en la tabla periódica
Tenga en cuenta que cuando consideramos los elementos que pertenecen a la misma familia en el lado izquierdo de la Tabla, el Los puntos de fusión y ebullición disminuyen a medida que aumenta el número atómico del elemento, es decir, de abajo a arriba. Esto se puede ver en los valores de los puntos de fusión y ebullición a 1 atm para los elementos de la familia 1 que se muestran a continuación:

Puntos de fusión y ebullición de los elementos de la familia 1
En el lado derecho de la Tabla Periódica ocurre lo contrario, la dirección de crecimiento del punto de fusión y ebullición de los elementos pertenecientes a la misma familia aumenta de arriba hacia abajo. Por lo tanto, los elementos con las temperaturas de fusión y ebullición más bajas se encuentran en la parte superior de la Tabla. La única excepción es el carbono, que tiene un punto de fusión de 3550 ° C y un punto de ebullición de 4287 ° C.
De lo contrario, la mayoría de los que tienen puntos de fusión y ebullición bajos son gases o líquidos a temperatura ambiente al nivel del mar. Como es el caso de los gases nobles, nitrógeno, oxígeno, flúor y cloro, que se encuentran en la parte superior derecha de la tabla.
Ahora, cuando se trata de elementos pertenecientes al mismo período (misma fila en la Tabla), vemos que los puntos de fusión y ebullición aumentan desde los lados hacia el centro de la Tabla. Vea el ejemplo de los elementos del segundo período:
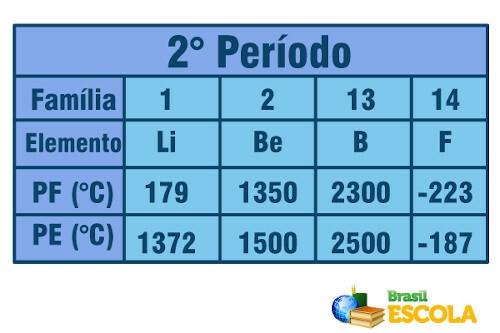
Punto de fusión y punto de ebullición de los elementos del segundo período de la tabla periódica
El tungsteno (W) es un elemento que se encuentra en el centro de la Tabla Periódica y su punto de fusión es el más alto entre los metales, siendo igual a 3422ºC. Por eso se utiliza en filamentos de bombillas incandescentes, ya que puede soportar altas temperaturas sin fundirse.
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/ponto-fusao-ebulicaopropriedades-periodicas.htm

