LA constante de hidrólisis (Kh) se refiere a un equilibrio químico establecido a partir de la hidrólisis de una sal (reacción química que involucra una sal soluble y agua).
Como constante de cualquier otro equilibrio, la expresión de constante de hidrólisis se construye a partir del producto de las concentraciones de producto dividido por el producto de las concentraciones de reactivo, como sigue:
Kh = [productos]
[reactivos]
Trabajar con la constante de hidrólisis implica el conocimiento de tres fenómenos importantes:
- Disociación de sales;
- Ionización de agua;
- Hidrólisis de sal.
Disociación de sales
Cuando se añade una sal soluble al agua, se disocia y libera un catión distinto del hidronio (H +) y un anión distinto del hidroxilo (OH-).

Para recordarle cuando una sal es o no soluble en agua, Haga clic aquí y estudiar la tabla de solubilidad de la sal.
ionización de agua
El agua es una sustancia que de forma natural sufre el fenómeno de autoionización, es decir, produce un catión hidronio y un anión hidroxilo.
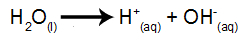
ecuación de ionización del agua
hidrólisis de una sal
Como sal soluble, libera iones en el agua y el agua sufre ionización, produciendo iones en el medio, puede tener lugar la reacción (hidrólisis) entre los iones de sal y los iones de agua. Cuando ocurre esta reacción, las posibles interacciones son:
- Catión de la sal con el anión de agua (formación de una base);
- Anión de sal con catión de agua (formación de una sal);
Las interacciones anteriores solo ocurrirán si la base o el ácido formado es débil.
Vea un ejemplo de la hidrólisis de una sal:
→ Hidrólisis de hipoclorito de amonio (NH4ClO)
Cuando se agrega hipoclorito de amonio al agua, se disuelve y se disocia, liberando los iones del catión amonio (NH4 +) y el anión hipoclorito (ClO-):

Ecuación que muestra los iones liberados en la disociación del hipoclorito de amonio
Como el agua, al someterse a ionización, produce H + y OH-, tenemos en la solución dos cationes y dos aniones, que pueden reaccionar. El catión NH4 + solo reacciona con el anión OH- porque forma una base débil (NH4OH). El anión ClO- solo reacciona con el catión H + porque forma un ácido débil (HClO).

Ecuación de equilibrio de hidrólisis de hipoclorito de amonio
Construcción de la expresión de la constante de hidrólisis
La construcción de la constante de hidrólisis de una sal depende exclusivamente de la ecuación de hidrólisis de esa sal. La hidrólisis del hipoclorito de amonio, por ejemplo, trabajado en el ítem anterior, generó la siguiente ecuación:

Ecuación de equilibrio de hidrólisis de hipoclorito de amonio
Cómo construir la expresión de constante de hidrólisis toma en cuenta productos y reactivos, la expresión de la constante sería:
Kh = [HClO]. [NH4OH]
[ClO -]. [NH4 +]
NOTA: El agua no participa en la ecuación porque es un reactivo líquido y también porque es el medio fundamental para que ocurra la hidrólisis, es decir, es constante.
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-constante-hidrolise.htm
