LA hidrólisis de sal entre ácidos y bases fuertes ocurre cuando el catión en una sal no interactúa con el anión en el agua y el anión en la sal no interactúa con el catión en el agua. La hidrólisis entre cationes y aniones de una sal y agua ocurre solo cuando el producto formado es un ácido débil, una base débil o ambos. Comprenda la hidrólisis de sal entre ácidos fuertes y bases fuertes paso a paso:
a) Paso 1: ionización de agua
El agua es una sustancia que tiene la capacidad de sufrir autoionización, es decir, produce catión hidronio (H+) y anión hidróxido (OH-) de su estructura.
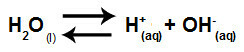
Ecuación que representa la autoionización del agua.
b) Paso 2: Disociación de sal
Cuando se agrega una sal al agua, pasa por el proceso de disociación. Como la sal es un compuesto iónico, en el agua, sus cationes y aniones se liberan en el medio, como se muestra en la siguiente ecuación:
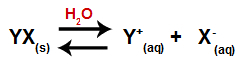
Ecuación que representa la disociación de cualquier sal.
c) Paso 3: Hidrólisis de sales de ácidos y bases fuertes.
Para ácido fuerte:
cuando el anión de la sal combinado con el H+ de agua para formar HCl, HBr, HI u otro ácido en el que la resta del número de oxígenos por el número de hidrógenos sea igual o superior a 2, tendremos un ácido fuerte. Por tanto, no se produce la combinación entre los iones mencionados.Para una base sólida: cuando el catión de la sal perteneciente a las familias IA (metales alcalinos) o IIA (metales alcalinotérreos distintos del magnesio) se combina con el OH- de agua, formará una base sólida. Por tanto, no se produce la combinación entre los iones mencionados.
Cuando los iones de sal no interactúan con los iones de agua, tenemos la siguiente ecuación:
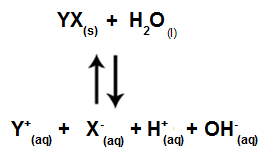
Ecuación que muestra todos los iones presentes en la solución.
En resumen, como los iones de sal no interactúan con los iones de agua, los iones de sal no promueven ningún cambio en la solución final. Por lo tanto, podemos escribir la ecuación de una hidrólisis de sal entre ácidos fuertes y bases fuertes solo con la ecuación de ionización del agua.
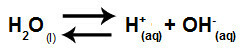
Ecuación que representa la hidrólisis de ácidos y bases fuertes.
d) Ejemplo de hidrólisis de sal entre ácidos y bases fuertes
Cuando agregamos la sal clorato de potasio al agua (KClO3), la sal se disocia y libera el catión potasio (K+) y el anión clorato (ClO3-) en el medio.
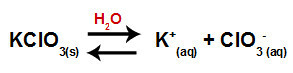
Ecuación de disociación para clorato de potasio
Es importante recordar que el agua se autoioniza y proporciona al medio catión hidronio (H+) y anión hidróxido (OH-). Ahora debemos evaluar la interacción entre los iones de sal y agua.
Cuando la H+ interactúa con ClO3-, forma ácido perclórico (HclO3). Dado que la resta del número de oxígenos por el número de hidrógenos ionizables en el ácido perclórico es 2, es fuerte. Por tanto, no se produce la interacción entre los iones.
Cuando el catión K+ interactúa con el anión OH-, tenemos la formación de una base fuerte, ya que el potasio es un metal alcalino. Por tanto, no se produce la interacción entre los iones.
La ecuación que representa la hidrólisis de la sal entre ácidos fuertes y bases a partir de la disolución del clorato de potasio en agua es:
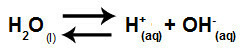
Ecuación química de la hidrólisis de clorato de potasio
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/hidrolise-salina-entre-acidos-bases-fortes.htm


