El volumen atómico no es el volumen que ocupa un átomo, sino que se refiere a la volumen ocupado por una cantidad fija de un número dado de átomos de un elemento químico.
En el texto Elemento químico, se demostró que un elemento corresponde a un conjunto de átomos que tienen el mismo número atómico, es decir, la misma cantidad de protones en el núcleo. La cantidad establecida para calcular el volumen atómico es el valor de Constante de Avogadro, que es igual a 6.02. 1023 átomos, que corresponde a 1 mol del elemento.
Entonces podemos decir que el volumen atómico es el volumen de 1 mol de átomos (o 6,02). 1023 átomos) de un elemento ocupa.
Esta cantidad se puede calcular si conocemos la densidad del elemento en estado sólido y la masa de 1 mol de átomos de ese elemento. Por ejemplo, considere que la densidad del sodio (Na) es igual a 0.97 g / cm3 y eso 6.02. 1023 Los átomos de sodio tienen una masa igual a 23,0 g. Entonces podemos, a partir de la fórmula de la densidad, llegar al volumen atómico del sodio. Ver cómo:
densidad = pasta
volumen
volumen atómico = masa de 6.02. 1023 átomos de elementos
densidad de elementos de estado sólido
Volumen atómico de sodio = 23,0 g
0,97 g / cm3
Volumen atómico de sodio = 23,71 cm3
El valor del volumen atómico involucra no solo el tamaño de los átomos, sino también la distancia entre ellos. Por tanto, dado que también se trata de espacios vacíos, no podemos tomar el valor del volumen atómico y dividir por el número de átomos (6.02. 1023) para encontrar el volumen que ocupa cada átomo.
Es importante estudiar el volumen atómico porque es una propiedad periódica, es decir, varía según el número atómico del elemento. Mira la imagen de abajo. El volumen atómico de los elementos. crece de arriba a abajo, lo que significa que cuando analizamos los elementos pertenecientes a la misma familia de la Tabla Periódica, a medida que crece el número atómico, también crece el volumen atómico. Esto se debe a que, en este sentido, los períodos aumentan, lo que significa que las capas electrónicas de los átomos aumentan y, en consecuencia, el volumen que ocupan también aumenta. Este es el mismo sentido de crecimiento que rayo atómico.
Por otro lado, horizontalmente, vemos que el volumen atómico aumenta desde el centro hacia los bordes. Cuando comenzamos desde la izquierda y vamos a la derecha hasta el centro de la tabla periódica, el volumen atómico disminuye porque el período es lo mismo, es decir, los elementos de la misma línea tienen la misma cantidad de capas electrónicas, pero el número atómico será creciente. Esto significa que la cantidad de electrones aumenta en esta dirección, lo que resulta en una mayor fuerza de atracción de electrones al núcleo del átomo, disminuyendo su radio atómico y, en consecuencia, el volumen atómico. Pero de centro a derecha, esto no sigue sucediendo, porque, en el caso de elementos ubicados en esta región, especialmente en el caso de los no metales, el espaciamiento entre sus átomos es relativamente grande, lo que afecta el volumen atómico, aumentando.
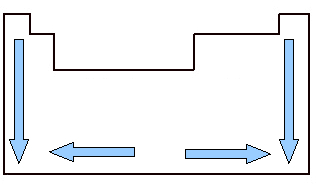
Variación del volumen atómico en la tabla periódica entre familias y períodos
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/volume-atomico.htm
