Vladimir Vasilyevich Markovnikov (1838-1904) fue un químico de Moscú que en 1869 comenzó a estudiar algunas reacciones de la adición de haluros de hidrógeno a alquenos y alquinos.
En estas reacciones, un alqueno reacciona con un haluro de hidrógeno o ácido halohídrico, como cloruro de hidrógeno (HCl), bromuro de hidrógeno (HBr) y yoduro de hidrógeno (HI). El producto formado a partir del alqueno es un haluro de alquilo, como enlaces de hidrógeno a uno de los carbonos del par y enlaces de halógeno al otro. Vea el ejemplo a continuación:
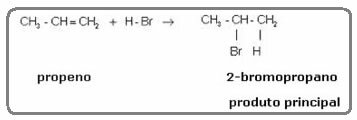
Algo similar ocurre también en la reacción de hidratación de los alquenos en medio ácido; en el que el producto formado es un alcohol:
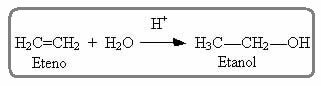
La molécula de etileno mencionada anteriormente es simétrica; por lo que no importa a qué carbono se agregarán el hidrógeno y el halógeno, respectivamente. Sin embargo, en moléculas asimétricas, como el propeno, cabría esperar la formación de dos posibles productos. Sin embargo, Markovnikov vio que esto no sucedía en la práctica. Para entender, mire la reacción a continuación:
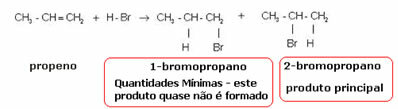
El producto formado prácticamente solo es 2-bromopropano. Y Markovnikov vio que esto también era cierto para otras sustancias. Entonces formuló la siguiente regla:

Lo mismo ocurre con la adición de agua. Debido a que tanto la molécula de agua como los haluros de hidrógeno son polares, el hidrógeno de estas moléculas adquiere un carácter electropositivo.
Hδ+_ X δ- y Hδ+_ Oh δ-
Al ser electropositivo, el hidrógeno se unirá al carbono más electronegativo, que será el que esté unido a la mayor cantidad de hidrógeno. Entonces tenemos:
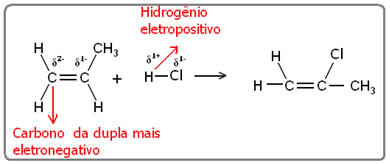
Por Jennifer Fogaça
Licenciada en Química
Equipo Escolar de Brasil
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/regra-markovnikov.htm

