se llama haz de iones el tamaño de un ion. El estudio de esta propiedad depende del conocimiento sobre el radio atómico y los iones.
Radio atómico: es una medida del tamaño de un átomo neutro (distancia teórica desde el núcleo hasta la última electrosfera).
iones: átomos que pierden (cationes) o ganan electrones (aniones).
Protones dentro del núcleo de un átomo ejercer una fuerza de atracción sobre los electrones (partículas negativas) presentes en las electroesferas. Cuanto mayor sea el número de protones, mayor será esta atracción y viceversa. Cuando el número de electrones en un átomo se modifica por una pérdida o ganancia de estas partículas, la atracción entre protones y electrones se modifica de la siguiente manera:
En el caso de un catión:
El número de electrones en las electroesferas se vuelve menor que el número de protones dentro del núcleo, el lo que hace que la fuerza de atracción del núcleo sea mayor, acercando los electrones a él. electroesferas. El resultado es una disminución del radio del átomo. Por tanto, el radio de un catión siempre será menor que el radio de su átomo neutro.
Radio del átomo neutro> Radio catiónico
En el caso de un anión:
El número de electrones en las electroesferas se vuelve mayor que el número de protones dentro del núcleo. En este caso, la fuerza de atracción que ejerce el núcleo es superada por la fuerza de repulsión entre los electrones presentes en las electrosferas, lo que da como resultado un aumento del radio del átomo. Por tanto, el radio de un anión siempre será mayor que el radio de su átomo neutro.
Radio de aniones> Radio de átomo neutro
Las dos situaciones que se presentan a continuación son un buen ejemplo de lo que sucede con el radio de un ion:
1 °) Átomo de sodio neutro (11Na) y el catión de sodio (11A+)
Mientras que el átomo de sodio neutro tiene once protones (esferas amarillas) y once electrones (esferas rojas), el catión de sodio tiene once protones y diez electrones.

Modelo de átomo neutro de sodio
Cuando el átomo de sodio neutro pierde un electrón, el radio disminuye.
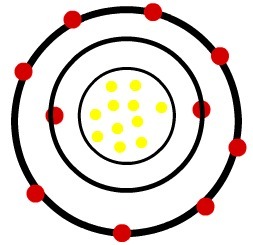
Modelo de un catión de sodio
Observación: El tercer nivel no estaba representado en la imagen del catión porque, al perder el único electrón que tenía, se vació y, por lo tanto, se descartó, pero está presente.
2o) Átomo neutro de fósforo (15P) y el catión fósforo (15PAG-3)
Mientras que el átomo de fósforo neutro tiene quince protones (esferas amarillas) y quince electrones (esferas rojas), el anión de fósforo tiene quince protones y dieciocho electrones.
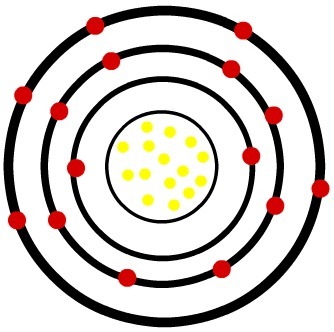
Modelo de un átomo de fósforo neutro
Cuando el átomo de fósforo neutro gana tres electrones, el radio aumenta.
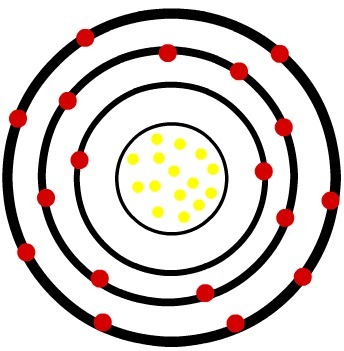
Modelo de un anión del fósforo.
Por mí. Diogo Lopes Dias
