Reacciones de desplazamiento, también llamado reacciones de sustitucióno todavía de intercambio simple, son aquellas que ocurren cuando una sustancia simple (formada por un solo elemento) reacciona con una sustancia compuesta, “desplazando” a esta última a una nueva sustancia simple.
Genéricamente, podemos definirlo de la siguiente manera:
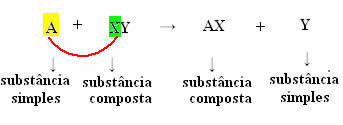
Pero para que esto suceda la sustancia simple, en el caso simbolizado por A, debe ser más reactivo que el elemento que será desplazado del compuesto, transformándose en una nueva sustancia simple (Y).
Veamos un ejemplo donde ocurre esta reacción:
Observe el experimento a continuación en el que se coloca una hoja de zinc (Zn) en una solución acuosa de sulfato de cobre (CuSO4). Con el tiempo, se observa que la solución de sulfato de cobre cambia de un color azul a un azul menos intenso, ya que se decolora y hay un depósito de cobre en la hoja de zinc.

Podemos representar esta reacción usando la siguiente ecuación química:

Tenga en cuenta que el zinc ha desplazado al cobre, lo que significa que el zinc es el más reactivo.
Dado que ambos son metales, podemos verificar si la reacción de intercambio simple ocurrirá o no analizando el cola de reactividad del metal mostrado a continuación:

Tenga en cuenta que el cobre es en realidad menos reactivo que el zinc, por lo que si decidimos hacer lo contrario del experimento anterior y Ponga una hoja de cobre en una solución de sulfato de zinc, la reacción no ocurriría, ya que el cobre no podría desplazar el zinc.
Las reacciones de desplazamiento son un tipo de reacción redox, ya que hay una transferencia de electrones de la sustancia simple a la compuesta. En el proceso explicado anteriormente, el zinc estaba inicialmente en su forma neutra, que es metálica, y se convirtió en parte de un compuesto en el que tiene una carga 2+, es decir, cada átomo de zinc ha perdido dos electrones. Con el cobre ocurre lo contrario, recibe dos electrones para pasar al estado sólido metálico.
En el caso de una reacción de intercambio simple con no metales, se considera: la reacción solo ocurrirá si el no metal más reactivo es la sustancia simple que puede desplazar a otro no metálico menos reactivo. La reactividad de los metales se muestra a continuación:

Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/reacoes-deslocamento-substituicao-ou-simples-troca.htm



