Entre las complejidades del estudio atómico está determinar el tamaño del átomo o, mejor, el rayo atómico. Esta propiedad periódica describe la distancia desde el núcleo hasta el electrón más externo de sus niveles electrónicos. Para determinarlo se realiza un promedio aritmético de la distancia entre los núcleos de dos átomos que forman una sustancia simple, por ejemplo.
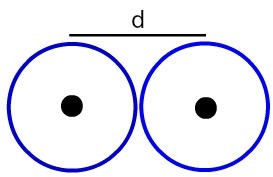
Representación de la distancia entre dos núcleos atómicos
Determinamos el radio atómico (RA) de los átomos ejemplificados en la imagen. Para hacer esto, simplemente divida la distancia entre los núcleos por 2:
RA = D
2
O estudio de rayos atómicos es importante porque favorece la comprensión de algunos eventos físicos (densidad, punto de fusión, punto de ebullición y energía de ionización) y productos químicos (enlaces químicos) que se producen con átomos.
Al analizar una tabla periódica, podemos evaluar si un átomo es más grande o más pequeño en relación con otro y, por lo tanto, determinar si tiene mayor o menor facilidad para eliminar uno o más electrones de sus orbitales. LA
evaluación y determinación del radio atómico en la tabla periódica se realiza de acuerdo con dos criterios básicos:a) Número de niveles de energía (familias o grupos / columnas verticales)
Sabemos que los átomos pueden tener hasta siete niveles de energía (K, L, M, N, O, P, Q) y que cada elemento químico se encuentra en familias o grupos (columnas verticales) y en períodos (columnas horizontal). Los períodos indican el número de niveles que tiene el átomo del elemento, y la familia indica el subnivel más energético del átomo. En un grupo o familia, los elementos químicos se diferencian por la cantidad de niveles de energía. Vea la tabla a continuación:

Cuanto mayor es el número de niveles de energía de un átomo, mayor es su radio atómico. Analizando la tabla anterior, se puede ver que el francio tiene el átomo más grande porque tiene siete niveles. El átomo de potasio, por otro lado, tiene un radio más pequeño ya que tiene cuatro niveles de energía. La siguiente es una representación comparativa entre el átomo de francio y el átomo de potasio:
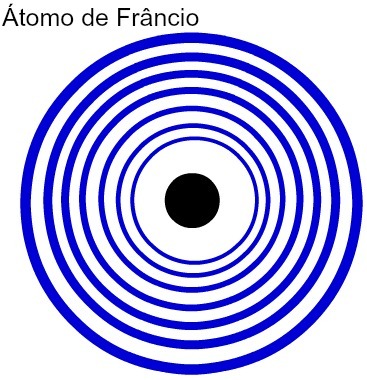
Representación de los siete niveles de energía del átomo de francio.

Representación de los cuatro niveles de energía del átomo de potasio.
El siguiente diagrama representa cómo ocurre el aumento del radio atómico en la misma familia o grupo (columnas verticales) de la tabla periódica. Cuanto mayor es el número de niveles, mayor es el radio, es decir, en la tabla periódica, el radio atómico crece de arriba hacia abajo:
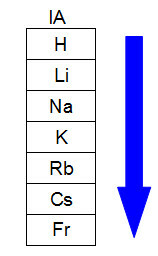
Representación de cómo aumenta el radio atómico en una familia de tablas periódicas
b) Número atómico (Z o número de protones) en el mismo período (columna horizontal)
Cuando los elementos químicos pertenecen al mismo período, sus átomos tienen la misma cantidad de niveles de energía, pero la cantidad de protones dentro de sus núcleos es diferente. La siguiente es una secuencia de elementos pertenecientes al cuarto período de la tabla periódica:
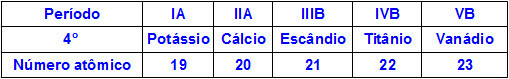
Todos los átomos de los elementos representados en la tabla anterior tienen cuatro niveles de energía, pero cada uno de ellos tiene una cantidad diferente de protones en sus núcleos. Como los protones dentro del núcleo ejercen una fuerza de atracción sobre los electrones presentes en los niveles de energía, cuanto mayor es la cantidad de protones en el núcleo, mayor es su atracción hacia los electrones. El resultado es una aproximación de los niveles hacia el núcleo, disminuyendo el tamaño del átomo.
↑Z = ↓ Radio atómico
↓Z = ↑ Radio atómico
Así, podemos afirmar que el radio atómico del elemento potasio es mayor que el del vanadio debido al menor número de protones.
El siguiente diagrama representa cómo aumenta el radio atómico en el mismo período (línea horizontal). Cuanto menor es el número atómico, mayor es el radio, es decir, el radio atómico en la tabla crece de derecha a izquierda.
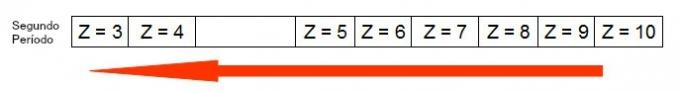
Representación de cómo aumenta el radio atómico en un período de la tabla periódica
Por mí. Diogo Lopes Dia