El estudio de la fuerza de un ácido es muy importante para determinar la capacidad de la solución ácida para conducir corriente eléctrica, ya que esto se relaciona con la cantidad de iones que esta sustancia produce cuando entra en contacto con el agua (ionización). Cuando un ácido es demasiado fuerte, produce demasiados cationes hidronio (H3O+) y muchos aniones (X-). Vea la ecuación de ionización del ácido bromhídrico:
HBr + H2O → H3O+ + Br-
Cuando se ioniza, el hidrógeno presente en la molécula de ácido interactúa con la molécula de agua y forma hidronio. Pero para que suceda este evento, el átomo de hidrógeno debe ser necesariamente ionizable. El hidrógeno ionizable es aquel capaz de formar un catión hidronio.. Para saber si un hidrógeno es ionizable, tenemos en cuenta la clasificación del ácido como hidrácido (no tiene oxígeno en su composición) u oxiácido (tiene oxígeno en su composición).
a) Hidrácidos
Todo el hidrógeno en un hidrácido se considera ionizable.
Ejemplos:
- HCl: un hidrógeno ionizable, produciendo así un hidronio;
- H2S: dos hidrógenos ionizables, luego producen dos hidrones
b) Oxiácido
En un oxiácido, solo el hidrógeno que está unido a un átomo de oxígeno en la molécula se considera ionizable. Para ello, es necesario construir su fórmula estructural. Vea algunos ejemplos:
H3POLVO4 (ácido fosfórico)
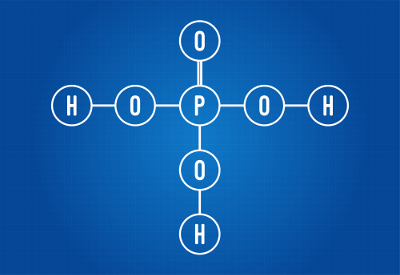
Fórmula estructural del ácido fosfórico
Podemos ver que, en la estructura del ácido fosfórico, hay tres hidrógenos unidos al oxígeno, por lo que hay tres hidrógenos ionizables. La ecuación de ionización será:
H3POLVO4 + 3 H2O → 3 H3O+ + PO4-3
H2SOLO4 (ácido sulfúrico)
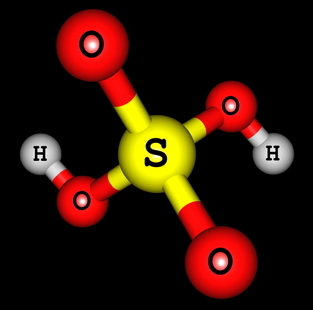
Fórmula estructural del ácido sulfúrico.
Podemos ver que, en la estructura del ácido sulfúrico, hay dos hidrógenos unidos al oxígeno, por lo que hay dos hidrógenos ionizables. La ecuación de ionización será:
H2SOLO4 + 2 H2O → 2 H3O+ + SO4-2
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm