El análisis de las propiedades físicas y químicas de los compuestos que realizan enlaces covalentes (al compartir electrones) nos muestra que existen grandes diferencias entre estos materiales. Pero antes de ver estas características en sí mismas, veamos cuál es la diferencia entre sustancias moleculares y covalentes.
A sustancias moleculares son las que se forman cuando los átomos se enlazan mediante enlaces covalentes, dando lugar a moléculas de un número determinado.
Sin embargo, el enlace covalente también puede originar compuestos en una estructura de red con un número muy grande e indeterminado de átomos, que son macromoléculas. Tales sustancias se llaman compuestos covalentes o sólidos de la red covalente. Algunos ejemplos de estos compuestos son: diamante (C), grafito (C), dióxido de silicio (SiO2) y carburo de silicio (SiC).
Ahora, veamos sus principales propiedades:
- Estado físico a temperatura ambiente: En condiciones ambientales, se encuentran compuestos moleculares y covalentes. en los tres estados físicos (sólido, líquido y gas).
Ejemplos:
O Sólido: azúcar (sacarosa), sílice (arena), diamante, grafito;
O Líquido: agua, acetona, etanol;
O Gaseoso: Sulfuro de hidrógeno, cloro gaseoso, bromo gaseoso, hidrógeno gaseoso.

- Punto de fusión y ebullición: En general, los puntos de fusión y ebullición de estas sustancias son más pequeños que los de las sustancias iónicas.
Las sustancias covalentes tienen temperaturas de ebullición más altas que las moleculares, siempre por encima de los 1000 ° C. Esto se debe a que a medida que sus moléculas están más unidas, formando redes cristalinas, es necesario aportar más energía para que cambien de estado.
Dos factores interfieren con los puntos de ebullición y fusión de compuestos covalentes y moleculares: a masa molar y el Fuerza intermolecular.
Cuanto mayor es la masa molar, mayor es la inercia de la molécula y, en consecuencia, mayor es el punto de ebullición y fusión. Si se aproximan las masas molares, observamos las fuerzas intermoleculares. La fuerza intermolecular más intensa es la del enlace de hidrógeno, que conduce a un punto de ebullición y fusión más alto. El intermedio es el dipolo permanente y el más débil, que conduce a un punto de ebullición y fusión más bajo, es el dipolo inducido.
- Corriente eléctrica: En su forma pura, tanto los líquidos como los sólidos no conducen una corriente eléctrica.
Una excepción es el grafito, que conduce la corriente eléctrica en forma sólida, porque sus electrones de doble enlace resuenan y por lo tanto tienen cierta movilidad.
- Solubilidad: Los polares se disuelven en polares y los no polares se disuelven en no polares.
- Tenacidad: La resistencia de las sustancias covalentes al impacto o choque mecánico es baja. En general, son sólidos quebradizos, como se muestra en el caso del vidrio, que está formado por silicatos de sodio y calcio.

- Tenacidad: En general, tienen una gran dureza. A excepción del grafito, porque sus átomos de carbono están ligados a otros tres átomos de carbono, formando placas hexagonales con cierta movilidad, haciéndolo blando. Por eso, incluso se utiliza como lubricante.
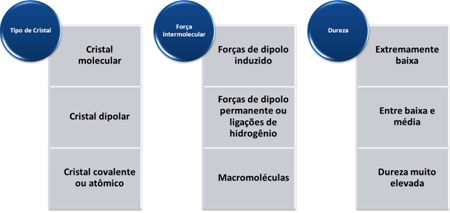
La dureza de estas sustancias varía según el tipo de cristal, como se muestra en la siguiente tabla:
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm
