EL rutherfordio es un elemento sintético de número atómico 104, perteneciente al grupo 4 de la Tabla periodica, siendo el primer miembro de la serie transactínida. Su primera detección data de 1964, en los famosos laboratorios de la ciudad de Dubna. Al igual que otros transactínidos, el nombre oficial del elemento 104 estuvo involucrado en un conflicto entre los soviéticos y los estadounidenses, en una pieza de la Guerra Fría en la historia de la química.
el rutherfordio no tiene aplicaciones practicas, dado que su isótopo más estable tiene unas dos horas y media de media vida. Sin embargo, estudios en sistemas y disoluciones gaseosas prueban su similitud química con los demás elementos del grupo 4, como el zirconio y el hafnio.
Lea también: Seaborgio: elemento sintético que lleva el nombre del científico Glenn Seaborg
Resumen de Rutherfordio
- Es un elemento químico sintético ubicado en el grupo 4 de la Tabla Periódica.
- Fue sintetizado por primera vez en 1964 en el Instituto Conjunto para la Investigación Nuclear en Dubna, Rusia.
- Es un elemento radiactivoabuela.
- Al igual que otros transactínidos, el rutherfordio adolece de baja estabilidad y es difícil sintetizar muestras considerables para estudios.
- Su nombre se hizo oficial recién en 1997, después de varios años de disputa entre los estadounidenses y los soviéticos.
Propiedades del rutherfordio
- Símbolo: RF
- número atómico: 104
- masa atomica: 267 c.u.s.
- Configuración electrónica: [Rn] 7s2 5f14 6d2
- isótopo más estable: 267Rf (2,5 ± 1,5 horas de vida media)
- serie química: grupo 4, transactínidos, elementos superpesados
Características de Rutherfordio
Como todos los transactínidos, es decir, elementos justo después de laurence (Lr), rutherfordio es un elemento radiactivo. Su isótopo más estable se detectó en 2004 y su vida media (el tiempo necesario para que la cantidad del radioisótopo caer a la mitad) es de dos horas y media, con un margen de error de una hora y media, más o menos.
La gran dificultad para establecer las características químicas del rutherfordio y otros transactínidos es, en general, el hecho de que hay una baja tasa de producción, ya sea en cantidad o en velocidad. En estos elementos, por ejemplo, es muy común evaluar químicamente un solo átomo, lo que, en cierto modo, requiere adaptaciones en cuanto a los cálculos, ya que la mayoría de las ecuaciones se establecen para sistemas con más de un átomo. Además, a menudo la Los isótopos tienen vidas medias muy cortas., lo que dificulta o incluso imposibilita estudios más profundos.
En el caso concreto del Rf, los científicos ya han conseguido demostrar que su comportamiento en fase líquida es similar al de otros elementos. grupo 4 más ligero, zirconio y hafnio, como en la formación de fluoruros en solución con posterior extracción en resinas de intercambio iónico. Este comportamiento ayudó a solidificar la presencia de rutherfordio en el grupo 4 de la Tabla Periódica.
Lee también: Nuevos elementos químicos: los cuatro elementos que faltan en el séptimo período
Obtención de rutherfordio
Los transactínidos necesitan una gran infraestructura para su producción. Todo se sintetizan con aceleradores de partículas, en el que especies iónicas chocan con elementos pesados. La detección de estos elementos tampoco es simple y directa.
Cuando se forma, el elemento radiactivo, por su propia naturaleza, comienza a decaer y exhibe emisiones, como partículas alfa y beta. A menudo es necesario evaluar la desintegración radioactiva del átomo formado o incluso identificar las especies atómicas que pueden surgir de estas reacciones nucleares, como en un rompecabezas.
Agregue esto al hecho de que las vidas medias de los isótopos de transactinida a menudo son cortas, en el rango de segundos, por lo que solo es posible obtener una cantidad en el rango de unos pocos átomos o incluso un solo átomo.
En el caso de Rf, la primera síntesis reportada para este elemento implicó la colisión de isótopos de plutonio, Pu, con iones de isótopo de neón 22, Eh.
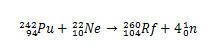
Sin embargo, se pueden producir otros isótopos de rutherfordio modificando las especies que colisionarán. Por ejemplo, el isótopo 261 puede producirse por la reacción entre el oxígeno-18 y el curio-248, produciendo cinco neutrones.
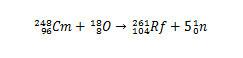
Míralo en nuestro podcast: ¿Cómo funciona un acelerador de partículas?
Precauciones con Rutherfordio
Dado que el rutherfordio ni siquiera se puede producir a una escala considerable, los riesgos asociados con este elemento están relacionados con la efectos de radiación. Sin embargo, en un laboratorio controlado, estos riesgos se anticipan y por lo tanto se minimizan.
Historia de Rutherfordio

Todos los transactínidos participaron en una carrera por su descubrimiento en las décadas de 1960 y 1970. Este episodio se reporta como el Guerra de Transferencias, una pieza de la Guerra Fría en la historia de la química. A pesar de llamarse así, lo que sugiere que las disputas ocurrieron por elementos posteriores al fermio, un elemento número atómico 100, los elementos directamente involucrados fueron 104 a 109, el recién descubierto transactinidas.
En el caso del rutherfordio, la disputa comenzó en 1964., cuando los investigadores soviéticos del Instituto Conjunto de Investigación Nuclear de la ciudad de Dubna Rusia, informó el descubrimiento del isótopo 260 del elemento 104 al bombardear plutonio-242 con iones neón-22. Pero los investigadores de Dubna solo presentaron una prueba, que fue la detección de un isótopo que ha decaído espontáneamente, sin identificar claramente su masa y su tiempo de media vida. Como resultado, el descubrimiento fue visto con recelo.
Cinco años más tarde, en 1969, un equipo de científicos estadounidenses del Laboratorio Nacional Lawrence Berkeley en Berkeley, California, dirigido por Albert Ghiorso, dijo que proporcionó evidencia suficiente para el descubrimiento del isótopo 257 del elemento 104 al colisionar californio-249 con carbono-12. Los mismos científicos pudieron producir más tarde el isótopo 259 del elemento 104. En 1973, los científicos del Laboratorio Nacional de Oak Ridge confirmaron de forma independiente la número atómico 104 para el isótopo de masa 257 producido en Berkeley.
Los años siguientes fueron de gran disputa entre los científicos de los dos países, hasta que, en 1985, se de Química Pura y Aplicada (IUPAC) y la Unión Internacional de Física Pura y Aplicada (IUAP) formar un comisión mixta de nueve científicos, llamada Grupo de Trabajo de Transferencias (Grupo de Trabajo de Transfermium o TWG). El TWG se creó para decidir quién era realmente responsable de los descubrimientos de los elementos que van del 101 al 112.
Aun así, las decisiones del TWG no siempre estuvieron libres de dudas. En el caso del elemento 104, el grupo de trabajo decidió que el El crédito debe ser compartido entre científicos soviéticos y estadounidenses., algo que no gustó nada a los científicos de Berkeley.
En 1991, Ghiorso y Seaborg, del equipo de Berkeley, llegaron a afirmar que la identificación del elemento 104 por parte de los científicos de Dubna era claramente equivocado y, en un momento, negó la validez de las conclusiones de TWG, considerándolas un perjuicio para la comunidad científico.
No es de extrañar, en A principios de la década de 1990, los nombres de los nuevos elementos aún no eran un consenso.. Luego hubo negociaciones que involucraron a científicos alemanes, rusos y estadounidenses, que resultaron frustradas. Allí, en 1992, el laboratorio alemán Gesellschaft für Schwerionenforschung (GSI) propuso nombres para los elementos 102 a 109, poniendo meitnerio para el elemento 104.
Aun así, la lista, a pesar de ser elogiada, no fue aceptada por los científicos involucrados. La decisión podría tomarse en 1994, durante la conferencia de la Comisión de Nomenclatura de Compuestos Inorgánicos (CNIC) de la Iupac. En él, se eligió el nombre dubnio para el elemento 104, sin embargo, la American Chemical Society adoptó, en el mismo año, el nombre rutherfordio para el elemento 104. el elemento 104, en un momento de descrédito por parte de los norteamericanos, quienes llegaron a cuestionar la autoridad de la IUPAC para formalizar nuevos nombres
solo en 1997, en la conferencia general de la IUPAC en Ginebra, es que el elemento 104 finalmente se hizo oficial como rutherfordio, después de que la ACS cediera en la nomenclatura de otros elementos cercanos.
Ejercicios resueltos en rutherfordio
Pregunta 1
El rutherfordio es un elemento sintético y una de las principales dificultades para estudiarlo es el hecho de que no es posible sintetizarlo en grandes cantidades.
Entre los posibles factores que contribuyen a esta dificultad, podemos señalar:
(A) Rutherfordio tiene isótopos de vida media larga del orden de millones de años.
(B) Rutherfordio se descompone espontánea y muy rápidamente, impidiendo la detección de sus cantidades macroscópicas.
(C) No existen tecnologías capaces de sintetizar el rutherfordio, siendo sus datos estrictamente teóricos y sin base científica.
(D) Las leyes de la química establecen que es imposible sintetizar elementos cuyo número atómico exceda el de Lawrence, 103.
(E) Durante la síntesis de rutherfordio, los elementos más ligeros de su grupo se priorizan químicamente.
Respuesta: letra b
Los elementos transactínidos, como el Rf, son radiactivos y se descomponen espontáneamente a gran velocidad, ya que su vida media es corta. Así, al final del experimento, quedan pocos átomos de las especies sintéticas.
Pregunta 2
En 1964, investigadores de Dubna afirmaron haber sintetizado el isótopo rutherfordio-260 (Z = 104). En el caso de este isótopo, ¿cuál es el número de neutrones?
(A) 104
(B) 260
(C) 151
(D) 156
(E) 161
Respuesta: letra D
El número de neutrones (n) se puede calcular, utilizando el número másico (A) y el número atómico (Z), a través de la siguiente ecuación:
A = Z + norte
Sustituyendo, tenemos:
260 = 104 + norte
n = 260 - 104
n = 156
créditos de imagen
[1] Abbas rosadas / obturador
Por Stefano Araújo Novais
Profesor de química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/rutherfordio-rf.htm


