reacciones con óxidos básicos Son fenómenos químicos en los que una sustancia de esta clase de óxidos se coloca en el mismo recipiente que un ácido inorgánico, a óxido de ácido o uno óxido anfótero.
Vea también:Reacciones con óxidos anfóteros
sal inorgánica y el agua son productos comunes en un reacción con óxidos básicos. Para saber si se producirá sal inorgánica o agua, debemos observar la sustancia que acompaña al óxido básico en el reactivo. Vea los ejemplos a continuación y comprenda cómo se lleva a cabo este proceso.
Reacciones con óxidos básicos y ácidos inorgánicos.
En las reacciones entre óxidos básicos y ácidos inorgánicos, se forman una sal inorgánica y agua, porque el catión óxido básico (Y+) interactúa con el anión (X-) del ácido, y el catión hidronio (H+) del ácido interactúa con el anión del óxido:
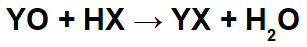
Ejemplo: Óxido de radio y ácido bromhídrico
En esta reacción, tenemos óxido de radio (RaO) y ácido bromhídrico (Hbr) como reactivos. Por lo tanto, ocurren las siguientes interacciones:
Catión de radio (Ra+2) con el anión bromuro (Br-1) formando la sal de bromuro de radio (RaBr2).
Catión hidronio (H+1) con el anión óxido (O-2) formando agua (H2O).
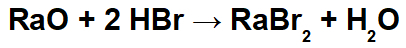
Vea también:Reacciones con óxidos dobles
Reacciones con óxidos básicos y óxidos ácidos.
En estas reacciones, se forma una sal inorgánica a través de la interacción entre el catión óxido básico (Y+) y el anión ácido resultante (WOlos-) de la reacción química entre un óxido de ácido y agua.
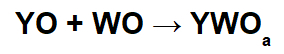
Ejemplo: Óxido de sodio y dióxido de azufre
En esta reacción, tenemos óxido de sodio (Na2O) y dióxido de azufre (SO2). Es de destacar que, inicialmente, cuando el óxido ácido interactúa con el agua, tenemos la formación de ácido sulfuroso (H2SOLAMENTE3):
No pares ahora... Hay más después de la publicidad;)

A partir de la formación de este ácido, la interacción entre el catión sodio (Na+1) del óxido básico y el anión sulfito (SO3-2) del ácido, formando la sal de sulfito de sodio (Na2SOLAMENTE3):
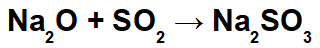
Reacciones con óxidos básicos y óxidos anfóteros.
Los óxidos anfóteros son sustancias que presentan un comportamiento químico dual: en presencia de una sustancia ácida, se comporta como un óxido básico; en presencia de una sustancia de naturaleza básica, se comporta como un óxido de ácido.
Entonces cuando un El óxido básico reacciona con un óxido anfótero., este se comportará como un óxido de ácido, formando un ácido inorgánico en presencia de agua. La reacción entre el anión del ácido inorgánico y el catión del óxido básico formará un producto de sal.
Ejemplo: Óxido de potasio y óxido de cromo III
En esta reacción, tenemos óxido de potasio como reactivos (K2O) y óxido de cromo (Cr2O3). Es de destacar que, inicialmente, cuando el óxido anfótero interactúa con el agua, tenemos la formación de ácido cromosómico (2HCrO2):

A partir de la formación de este ácido se produce la interacción entre el catión potasio (K+1) del óxido básico y el anión cromita (SO3-2) del ácido, formando la sal de cromito de potasio (2KCrO2):

Por mí. Diogo Lopes Dias
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
DÍAS, Diogo Lopes. "Reacciones con óxidos básicos"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/reacoes-com-oxidos-basicos.htm. Consultado el 27 de julio de 2021.
Nomenclatura de la sal, clasificación de la sal, nombre del anión, nombre del catión, sulfato de hierro, sulfato ferroso, nitrato de plata, cloruro de potasio, cloruro de sodio, cloruro de calcio, nitrato de plata, sulfato de cobre, carbonato calcio.