Los compuestos orgánicos son moleculares, es decir, sus átomos llevan enlaces covalentes entre sí. Cuando analizamos los enlaces entre carbonos, que pueden ser simples, dobles o triples, observamos que son enlaces no polares, ya que no hay diferencia en electronegatividad entre los átomos, ya que pertenecen al mismo elemento.
Además, dado que el hidrógeno y el carbono tienen una diferencia de electronegatividad muy pequeña, los enlaces entre ellos también son no polares.
Conexiones no polares:
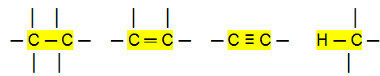
Con eso, podemos concluir que el Hidrocarburos (compuestos orgánicos que solo tienen átomos de carbono e hidrógeno) son moléculas no polares. En estos compuestos, la interacción intermolecular es del tipo dipolo inducido, que es el más débil que existe.
Dado que son débiles, estas interacciones son fáciles de romper. Debido a eso, las temperaturas de ebullición y fusión de los hidrocarburos son más bajas que las de otras funciones.

Comparando hidrocarburos, los puntos de ebullición aumentarán a medida que aumente la masa molar.
Por ejemplo, el etano y el butano son ambos alcanos. Vea los puntos de ebullición de cada uno determinado experimentalmente:
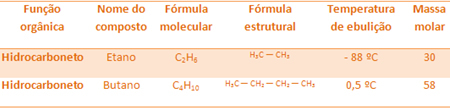
Tenga en cuenta que la temperatura de ebullición del butano es mucho más alta que la del etano, ya que su masa molar también es más alta.
Ahora, cuando comparamos hidrocarburos que tienen la misma masa molar (son isómeros), pero que tienen diferentes tipos de cadenas de carbono, nos damos cuenta de que cuanto mayor sea el número de ramas, menor será la temperatura de ebullición, porque la estructura de la molécula se vuelve más compacta, es decir, su superficie disminuye.
Todos los alcanos siguientes tienen la misma fórmula molecular, C5H12, pero sus temperaturas de ebullición son diferentes:
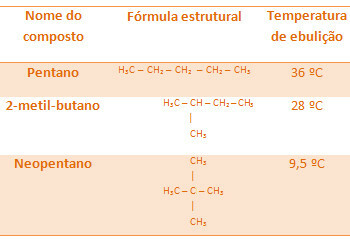
Tenga en cuenta que la temperatura de ebullición del neopentano es la más baja ya que tiene más ramas.
Podemos considerar que las demás funciones orgánicas se derivan de los hidrocarburos, mediante la sustitución de uno o más hidrógenos por átomos o grupos de átomos de otros elementos. Generalmente, las otras funciones orgánicas tienen oxígeno o nitrógeno, que son elementos más electronegativos que el carbono. Atraen con más fuerza el par de electrones compartidos con el carbono y, por lo tanto, hacen que la molécula sea polar:
Conexiones polares:
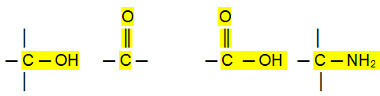
Los aldehídos, cetonas y haluros orgánicos tienen puntos de ebullición más altos que hidrocarburos, porque su interacción intermolecular es el dipolo permanente, que es más fuerte que el de dipolo inducido.
Los alcoholes, ácidos carboxílicos y aminas, por otro lado, tienen temperaturas de ebullición aún más altas, ya que llevan a cabo enlaces de hidrógeno, el tipo más intenso de interacción intermolecular.
En compuestos de todas estas funciones, se aplica lo mismo que vimos para los hidrocarburos:

Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/polaridade-temperatura-ebulicao-dos-compostos-organicos.htm
