Una reacción de neutralización ocurre cuando un ácido reacciona con una base para formar agua y sal. El ácido proporciona los iones H+ y la base proporciona los iones OH- para la formación de agua (H2O):
1 hora+(aquí) + 1 OH-(aquí) → H2O(ℓ)
Este tipo de reacción se denomina "neutralización" porque el pH del medio se neutraliza; el pH del agua es 7.0 (neutro).
Para que ocurran estas reacciones es necesario liberar una cierta cantidad de calor, ya que solo una parte de la energía del Los iones se utilizan para formar los enlaces que dan como resultado moléculas de agua, mientras que el resto de la energía se libera al bastante. Esta energía liberada se llama Entalpía de neutralización (∆Hneutralización).

Dado que libera calor, corresponde a reacciones exotérmicas, en las que la entalpía (energía global del sistema) siempre será negativa, menor que cero.
En el caso de una reacción entre ácidos fuertes y bases fuertes, el valor de entalpía de neutralización siempre será igual a - 13,8 kcal / mol o - 57,7 kJ / mol. Esto sucede porque las bases y los ácidos fuertes están completamente disociados en solución y, por lo tanto, el único La reacción responsable de la manifestación del calor será la formación de agua, como se muestra en los tres ejemplos siguientes:
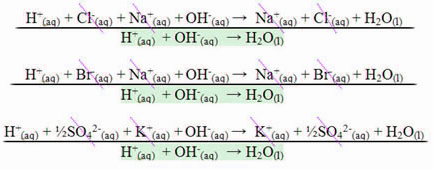
En el caso de reacciones de neutralización en las que intervengan ácidos o bases débiles, el valor de entalpía de neutralización será inferior a –57,7 kJ / mol.
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm
